Анодная кривая
Cтраница 2
Анодные кривые перенапряжение - In г, полученные в работах Браттена и Гарретта [66] и Тернера [80], имеют в тафелевской области наклон, равный 2RT / F, причем различия в io для п - и р-германиевых электродов не наблюдались. При плотности тока - 10 - 3 а-слг 2 перенапряжение на гс-германиевом электроде повышается значительно быстрее, чем 2 303 ( 2RT / F) вольт при десятикратном увеличении тока. [16]
Анодные кривые перенапряжение - In i, полученные в работах Браттена и Гарретта [66] и Тернера [80], имеют в тафелевской области наклон, равный 2RT / F, причем различия в 10 для п - и р-германиевых электродов не наблюдались. При плотности тока - 10 - 3 а слг2 перенапряжение на гс-германиевом электроде повышается значительно быстрее, чем 2 303 ( 2RT / F) вольт при десятикратном увеличении тока. [17]
Анодные кривые вследствие отсутствия поляризации имеют очень пологий вид, что характеризует отсутствие пассивности и протекание коррозионного процесса без заметного торможения. Кривые катодной поляризации во всех случаях имеют относительно большую крутизну, что указывает на возможность прекращения или значительного торможения процесса коррозии образца при катодной поляризации. [18]
Анодная кривая ( E ai) может пересекать суммарную катодную кривую в области, расположенной ниже уровня, отвечающего E ai, тогда защита будет неполной ( рис. 20), хотя коррозионный ток несколько снизится. [20]
Анодные кривые снимают в потенциодинамическом режиме при скорости наложения потенциала 8 - 10 мВ / с. Поляризационные кривые строят в координатах Eaf ( ia) на одном графике. Делают выводы о влиянии хлорид-иона на анодный процесс. [21]
Анодные кривые снимают в потенциодинамическом режиме при скорости наложения потенциала 8 - 10 мВ / с. Делают выводы о влиянии хлорид-иона на анодный процесс. [22]
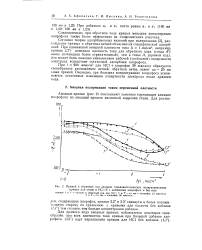 |
Прямой и обратный ход анодных гальваностатических поляризационных кривых для стали в НС1 IN с добавками хлорофоса и без них. [23] |
Анодные кривые ( рис. 2) показывают заметное тормозящее влияние хлорофоса на анодный процесс кислотной коррозии стали. [24]
Анодные кривые потенциал - плотность тока для никеля, полученные потенциоста-тическими, потенциокинетическими и в ранних исследованиях гальваностатическими методами, публиковали многие авторы. К сожалению, данные различных работ не всегда хорошо согласуются. [26]
Анодные кривые снимают в потенциодинамическом режиме при скорости наложения потенциала 8 - 10 мВ / с. Поляризационные кривые строят в координатах Esf ( ia) на одном графике. Делают выводы о влиянии хлорид-иона на анодный процесс. [27]
 |
Поляризационная кривая для типичных случаев контроля электрохимической коррозии. [28] |
Анодная кривая AiQ пересекает катодную кривую EUQ PQMN в точке Q при токе, меньшем половины предельного тока кислородной деполяризации Id - Отношение поляризации катода к поляризации анода AEKI / EAI велико, что указывает на отсутствие анодной пассивности. [29]
Обобщенная анодная кривая для металла, способного переходить в пассивное состояние, схематично представлена на рис. 1.2. На этой кривой имеются характерные точки: фа - равновесный потенциал анодной реакции в данном электролите; фст - стационарный потенциал металла в данной среде ( потенциал коррозии); фп - потенциал пассивации; фпп - потенциал полной пассивации; inn - плотность тока пассивации; iK - плотность тока полной пассивации; ( к - ток коррозии. [30]
Страницы: 1 2 3 4 5

