Центральный атом
Cтраница 1
 |
Экстракция кобальта трибутилфосфатом из растворов СаС12 ( 1, LiCl ( 2 и НС1 ( 3. [1] |
Центральный атом может иметь координационное число 4 ( тетраэдр) или 6 ( октаэдр) в зависимости от ряда факторов и природы растворителя, температуры и др. В одной и той же экстракционной системе кобальт при разных условиях может извлекаться по различным механизмам, например, в виде координационно сольватированной соли СоС12 - 2ТБФ при низких концентрациях хлорид-ионов и в виде комплексной кислоты Н2СоС14 - при высоких. Существенно, что прочность галогенид-ных комплексов кобальта и никеля значительно различается ( никель образует крайне неустойчивые комплексы); это позволяет разделять названные элементы. [2]
Центральный атом наиболее ненасыщен; поэтому естественнее всего допустить, что соединение двух частиц происходит в первую фазу при посредстве этих атомов. Очевидно, скорость полимеризации при прочих равных условиях должна быть пропорциональна степени ненасыщенности центрального атома. [3]
 |
Слой молекул Н2О в структуре. [4] |
Центральный атом является металлическим атомом. [5]
Центральный атом может быть атомом переходных и непереходных металлов, хотя большинство исследований было выполнено с первыми из них. Детальное изучение было проведено лишь в очень редких случаях. [6]
Центральный атом называется различно - в зависимости от того, входит ли он в состав комплексного катиона, комплексного аннона или комплексной нейтральной молекулы. [7]
Центральный атом может частично акцептировать на вакантные d - орбитали свободные электронные пары галогена. [8]
Центральный атом не может нести столь большой заряд, как предполагалось бы для большого числа ковалентных связей, так как образование каждой связи означает внедрение еще одного электрона в d - орбиту центрального атома. В данном случае необходима либо большая степень ионного характера ковалентных связей, благодаря чему электроны ( вследствие разности в электроотрицательностях) оттягиваются, от металла, либо какая-то двоесвязанность. Если мы попытаемся представить себе наличие шести СН3 - групп, октаэдрически расположенных вокруг гибридизованного атома переходного металла, то разность в электроотрицательностях недостаточна для того, чтобы достигнуть 50 % ионности связи, что наблюдается в связи Со-N. Следовательно, если какая-либо металлоорганическая связь и может вообще образоваться с переходными металлами, то, по всей вероятности, она способна образовываться только с наиболее отрицательными органическими группами. Подобное же заключение было сделано Германом и Нельсоном [15] на основании совершенно иных доводов и было подтверждено их опытами, касающимися стабильности связи титан - углерод: монофенилтитантрихлорид или монофенилтитантриалкоксипро-изводные устойчивы в течение нескольких часов, а фенилтри-изопропоксититан можно выделить, в то время как этилтитано-вые соединения обладают чрезвычайно малой жизнеспособностью даже при низких температурах. Продуктами разложения неизменно являются производные восстановленной формы титана. [9]
Центральный атом Со, расположенный в центре инверсии, связывает эти фрагменты, образуя связи с шестью атомами О: по одному от каждого лиганда. [10]
Центральные атомы в многоядерных комплексных соединениях могут быть связаны непосредственно между собой или через лиганды. [11]
Центральные атомы в многоядерных комплексных соединениях могут быть связаны между собой непосредственно. Такие соединения принято называть кластерными. В них могут присутствовать и мостиковые лиганды. [12]
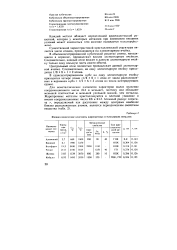 |
Физико-химические константы жаропрочных и тугоплавких металлов. [13] |
Центральный атом полностью принадлежит данной элементарной ячейке. Следовательно, на одну элементарную ячейку приходится 1 / 8x8 12 атома. [14]
Центральный атом также называют комплексообразователем. В химии слово координировать употребляют в смысле располагать около координационного центра. [15]
Страницы: 1 2 3 4