Кристалл - ромбическая система
Cтраница 1
Кристаллы ромбической системы имеют три взаимно перпендикулярные оси второго порядка. Характеристическая поверхность тензора a j может быть произвольной поверхностью второго порядка, главные оси которой параллельны осям кристалла. Тензор а-у может иметь три различных собственных значения. [1]
Мелкжэ кристаллы ромбической системы в виде игл или листочков с шелковистым блеском. Расплавленный РЬС12 при охлаждении затвердевает в белую роговидную массу. [2]
Обычно получают кристаллы ромбической системы возгонкой в атмосфере инертного газа, при температуре темно-красного каления могут образовываться кристаллы кубической системы. Полученный осаждением Sb2O3 представляет собой тонкий белый порошок пл. При нагревании препарат желтеет, при остывании снова становится белым. При 655 С плавится в желтоватую или серую жидкость, которая при охлаждении затвердевает в белую, асбестоподобную массу с шелковистым блеском. При более высокой температуре ( без доступа воздуха) сурьмянистый ангидрид возгоняется. [3]
Обычно получают кристаллы ромбической системы возгонкой в атмосфере инертного газа, при температуре темно-красного каления могут образовываться кристаллы кубической системы. Полученный осаждением Sb203 представляет собой тонкий белый порошок пл. При нагревании препарат желтеет, при остывании снова становится белым. При 655 С плавится в желтоватую или серую жпд-кость, которая при охлаждении затвердевает в белую, асбестоподобную массу с шелковистым блеском. При более высокой температуре ( без доступа воздуха) сурьмянистый ангидрид возгоняется. [4]
Обычно получают кристаллы ромбической системы возгонкой в атмосфере инертного газа, при температуре темно-красного каления могут образовываться кристаллы кубической системы. Полученный осаждением Sb2O3 представляет собой тонкий белый порошок пл. При нагревании препарат желтеет, при остывании снова становится белым. При 655 С плавится в желтоватую или серую жидкость, которая при охлаждении затвердевает в белую, асбестоподобную массу с шелковистым блеском. При более высокой температуре ( без доступа воздуха) сурьмянистый ангидрид возгоняется. [5]
Покажите, что кристаллы ромбической системы имеют девять независимых упругих податливостей. [6]
Мелкие бесцветные или слабо-желтоватые кристаллы ромбической системы или лучисто-кристаллическая масса. Реактив хорошо растворим в воде ( 44 9 % при 19 С), очень мало растворим в абсолютном этиловом спирте. Проявляет свойства окислителя и восстановителя. [7]
Наконец, в кристаллах ромбической системы фиксировано положение всех трех главных осей - они должны совпадать с тремя взаимно перпендикулярными осями симметрии второго порядка. [8]
Наконец, в кристаллах ромбической системы фиксировано положение всех трех главных осей - они должны совпадать с тремя взаимно перпендикулярными осями симметрии второго порядка. [9]
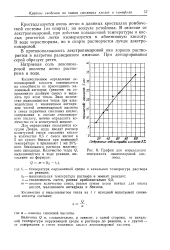 |
График для определения содержания левопимаровой кислоты. [10] |
Кристаллизуется очень легко в длинных кристаллах ромбической системы ( из спирта); на воздухе устойчива. В отличие от декстропимаровой, при действии повышенной температуры и кислых реагентов легко изомеризуется в абиетиновую кислоту. В воде нерастворима, но в спирте растворяется лучше декстропимаровой. [11]
Хрупкие темно-серые с металлическим блеском кристаллы ромбической системы. Пары иода имеют фиолетовый цвет. Задах неприятный, несколько похожий на хлор. [12]
Хрупкие темно-серые с металлическим блеском кристаллы ромбической системы. Пары иода имеют фиолетовый цвет. Запах неприятный, несколько похожий на хлор. [13]
Средний крон осаждается в виде кристаллов ромбической системы, но при пребывании в маточном растворе и промывке происходит перекристаллизация в моноклинную систему. Темный крон стремятся сразу получать в моноклинной системе. Светло-лимонный крон остается в ромбической системе и после сушки. [14]
Оба они являются в природе в кристаллах ромбической системы, и, что всего важнее, в серебряно-медном блеске находится изоморфная смесь их обоих, сохраняющая форму медного блеска, при различных отношениях меди к серебру, а - потому имеющая состав R3S, где R Си, Ag. При сходстве атомного состава соединений закиси меди СиХ и окиси серебра AgX с соединениями щелочных металлов КХ, NaX, представляется, однако, и значительная мера разницы между этими двумя разрядами элементов. Эта разность видна ясно в том, что щелочные металлы принадлежат к числу элементов, чрезвычайно легко соединяющихся с кислородом и разлагающих воду, тогда как серебро и медь трудно окисляются, образуют основания менее энергические и воды не разлагают не только при обыкновенной температуре, но даже при довольно возвышенной, даже из немногих только кислот выделяют водород. Различие тех и других видно, далее, в неодинаковости свойств многих соответственных соединений. Так, СиЮ и AgaO в воде нерастворимы, углекислые соли, хлористые металлы и сернокислые соли закиси меди и окиси серебра также мало растворимы в воде. Окислы серебра и меди притом легко восстановляются. Эта разность в свойствах находится в тесном отношении к тому различию плотности металлов, какое здесь существует. Щелочные металлы принадлежат к числу легчайших, медь и серебро - к числу тяжелейших, а потому объем атома этих двух классов металлов весьма неодинаков, а именно - для первых большой, для вторых малый ( таблица [ на ] стр. Медь принадлежит к числу немногих металлов, давно известных в металлическом виде. [15]
Страницы: 1 2 3 4