Кристалл - сульфат - кальций
Cтраница 3
Рассмотрим процесс возникновения кристаллических пленок на гранях кристаллов сульфата кальция и поверхности частиц апатита. Условием образования таких пленок является создание пересыщения раствора по пленкообразующему веществу. Пересыщение в производственном процессе возникает в результате химической реакции или изменения температуры. [31]
 |
Зависимость седиментационного объема суспензий V и высоты осадка h от времени т. [32] |
На фильтрующие свойства фосфорнокислых суспензий помимо качества кристаллов сульфата кальция влияют: отношение жидкость - твердое ( Ж: Т) в пульпе, вязкость жидкой фазы пульпы, толщина слоя образующегося осадка и разрежение. [33]
 |
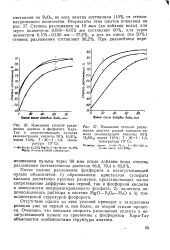
Зависимость коэффициента извлечения ( Лиэвл от времени разложения ( т и содержания H2SO4 ( Сн, so4 фи 70 С ( содержание Р2О5 в растворе 30 %. [34] |
В процессе кристаллизации чрезвычайно важно обеспечить получение крупных изометрических кристаллов сульфата кальция, обладающих хорошей фильтрующей способностью. Кристаллообразование сульфата кальция начинается из пересыщенных растворов с появления центров кристаллизации ( зародышей), на поверхности которых начинается рост кристаллов. Очевидно, что образование меньшего числа зародышей обеспечивает, при прочих равных условиях, образование более крупных кристаллов. [35]
Можно полагать, что адсорбированный магний в кристалле сульфата кальция, по-видимому связанный с сульфат-ионом в виде MgS04, ухудшал структуру осадка и, следовательно, его фильтруемость. [36]
Исследованиями азотно-сернокислотного способа [104] установлено, что хорошо фильтрующиеся кристаллы сульфата кальция образуются при циркуляции части конечного раствора, возвращаемого в процесс для разбавления реак-циолной массы. [37]
Показано, что в результате конверсии получаются хорошо фильтрующие кристаллы сульфата кальция. [38]
Отличительная особенность процесса - выделение крупных, хорошо фильтрующих кристаллов сульфата кальция, что объясняется малым пересыщением жидкой фазы этой солью из-за увеличения растворимости ее в фосфорнокислых растворах, содержащих азотную кислоту [37, 38], а также уменьшением вязкости растворов. [39]
Надо сказать, что большая часть работ по модификации формы кристаллов сульфата кальция связана с гипсом. Полугидрату и ангидриту в этом отношении уделялось значительно меньше внимания. Из растворов химически чистой фосфорной кислоты полугидрат осаждается в виде иглообразных кристаллов. Из экстракционной фосфорной кислоты выделяются кристаллы CaSO4 - 0 5H2O, имеющие форму шестигранных призм [17], которые частично собраны в крупные сростки. Состоящий из агрегатов осадок полугидрата легко отделяется от маточного раствора. Сростки кристаллов CaSO4 - 0 5Н2О достигают довольно больших размеров - 200 - 350 мкм. [40]
В сочетании с ионами алюминия благоприятное влияние на форму и размеры кристаллов сульфата кальция оказывают ионы кремнефторида. При наличии в растворе большого количества кремневой кислоты гипс кристаллизуется в виде тончайших игл. Кроме того, выделившаяся при экстракции фосфорной кислоты из некоторых фосфоритов кремневая кислота в виде илистого осадка сильно затрудняет отделение жидкой фазы от твердой. [41]
Таким образом, одним из направлений улучшения вяжущих свойств кремнегипса является укрупнение кристаллов сульфата кальция в процессе его образования, что позволяет резко сократить расход воды при затворении и повысить прочность. [42]
Почти полное разложение фосфорита в незагустевающей пульпе объясняется: 1) образованием кристаллов сульфата кальция достаточно крупных размеров, представляющих малое сопротивление диффузии как серной, так и фосфорной кислоты к поверхности непрореагировавшего фосфата; 2) наличием не-донасыщенного раствора в системе MgO-PsOs - Н2О и 3) тонкодисперсной структурой фосфорита. [44]
Почему в производстве экстракционной фосфорной кислоты необходимо добиваться минимального расхода воды при, промывке кристаллов сульфата кальция. [45]
Страницы: 1 2 3 4 5