Кристалл - хлорид
Cтраница 3
Так, например, при наличии смеси сходных бесцветных ( в видимой области) кристаллов хлорида и бромида свинца можно обнаружить в ультрафиолетовой области одновременно оба соединения, так как хлорид свинца не поглощает ультрафиолетовых лучей вблизи видимой области, а бромид свинца обладает сильным поглощением. [31]
После высыхания оставшейся жидкости желатина образовывала на поверхности держателя тонкий и равномерный слой, окружающий кристаллы хлорида серебра. [32]
При сплавлении ангидридов а - или о-дикарбоновых кислот с резорцином или 2 6-диоксипиридином 12 в присутствии кристалла хлорида цинка образуются фталеины, растворяющиеся в щелочах с зеленой или синей флуоресценцией. Эта реакция недостаточно надежна, так как и другие соединения, такие, как лимонная, винная кислоты, глицерин и глюкоза, дают подобные окраски. [33]
В табл. 16 сопоставлены вычисленные и экспериментально определенные магнитные моменты ионов - элементов четвертого периода в кристаллах хлоридов, нитратов, сульфатов и других солей, а также в их водных растворах. [34]
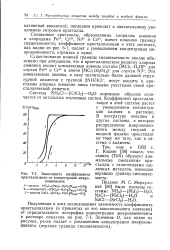 |
Зависимость коэффициента кристаллизации от концентрации микрокомпонента. [35] |
Эти комплексные анионы, в силу значительно более далекой структурной аналогии с группой 2NHJ4C1 -, могут входить в кристаллы хлорида аммония лишь готовыми участками своей кристаллической решетки. [36]
После добавления хлорида натрия в количестве, превышающем эквимолекулярное по сравнению с количеством нитрата серебра, в растворе возникает избыток СГ-ионов, которые сорбируются кристаллами хлорида серебра, и мицелла заряжается отрицательно. Адсорбционный и диффузный слой занимают катионы натрия, а анионы примулина десорбируются и поэтому вновь возникает флуоресценция. [37]
После добавления хлорида натрия в количестве, превышающем эквимолекулярное по сравнению с количеством нитрата серебра, в растворе возникает избыток С1 - ионов, которые сорбируются кристаллами хлорида серебра, и мицелла заряжается отрицательно. Адсорбционный и диффузный слой занимают катионы натрия, а анионы примулина десорбируются и поэтому вновь возникает флуоресценция. [38]
Стальные футерованные аппараты с успехом могут быть использованы также для очистки раствора хлорида марганца от хлоридов других металлов, для сбора и1 хранения очищенных и упаренных растворов, а также маточников, отделенных от кристаллов хлорида марганца на стадии кристаллизации. Опыта применения стали ОХ23Н28МЗДЗТ и титана ВТ1 для изготовления аппаратов упаривания раствора хлорида марганца и других близких по свойствам хлоридов не имеется, поэтому указанные материалы должны быть вначале испытаны в опытнопромышленном масштабе. [39]
Просветление изделий из кристаллов, прозрачных для ИК излучения, при помощи окисных пленок не всегда возможно. Кристаллы хлоридов, фторидов, бромидов и иодидов щелочных металлов не достаточно термоустойчивы, а нанесение пленок окислов толщиной более микрометра осуществимо лишь при высокотемпературной обработке. Коэффициенты линейного термического расширения окислов металлов и кристаллов резко различны, что также затрудняет применение с этой целью неорганических пленкообразующих веществ. [40]
Образовавшийся раствор фильтруют и упаривают под тягой в фарфоровой чашке до тех пор, пока проба раствора не начнет кристаллизоваться при охлаждении ( пробу брать стеклянной палочкой на часовое стекло), после этого чашке дают остыть. Кристаллы хлорида бария отфильтровывают на воронке Бюхнера, взвешивают и рассчитывают выход продукта в процентах. [41]
В каплю, после осаждения гипса, вводят кристалл TINOs. Выпадают кристаллы хлорида таллия ( см. рис. 250, стр. [42]
Несколько кристаллов хлорида аммония поместите в цилиндрическую пробирку и укрепите ее в штативе почти горизонтально. Очень маленьким пламенем горелки нагревайте дно пробирки только в том месте, где лежит соль, стараясь сохранить холодной верхнюю часть пробирки. [43]
Вещества, растворы которых проводят электрический ток, называются электролитами. Вода и кристаллы хлорида меди практически не проводят электрический ток. Раствор хлорида меди в воде является хорошим проводником. При прохождении электрического тока через водный раствор хлорида меди у положительного электрода, называемого анодом, выделяется газообразный хлор. На отрицательном электроде, называемом катодом, выделяется медь. [44]
В пробирку вносят 3 капли раствора хлорида кобальта ( П) и медленно, по каплям прибавляют раствор аммиака до выпадения синего осадка CoOHCl. Добавляют несколько кристаллов хлорида аммония и продолжают прибавление раствора аммиака при перемешивании смеси до полного растворения осадка и образования желтого раствора. При стоянии на воздухе раствор постепшно меняет окраску на вишнево-красную. [45]
Страницы: 1 2 3 4