Кристалл - благородный газ
Cтраница 1
Кристаллы благородных газов также молекулярные, построены из одноатомных молекул. Первые состоят из одинаковых молекул, вторые-из разных. [1]
Для кристаллов благородных газов и ионных кристаллов аналогичных экспериментальных данных получено очень мало, однако поверхностную энергию таких кристаллов можно рассчитать, введя электростатический потенциал для взаимодействия атомов или ионов. [2]
Ван-дер-ваальсово взаимодействие связывает кристаллы благородных газов и молекулярные кристаллы при низких температурах. Слабость ван-дер-ваальсова взаимодействия объясняет низкую температуру плавления таких кристаллов. Примеры молекулярных кристаллов - твердые Н2 и N2 и многие органические кристаллы. Элементарными кирпичиками молекулярных кристаллов являются молекулы, расстояния между которыми больше, чем расстояние между атомами в каждой молекуле. [3]
Значения энтропии плавления кристаллов благородных газов называют в свою очередь что следует также учитывать такие лады в изменение энтропии при плавлении, которые обусловлены юцессами разупорядочения, рассмотренными несколько выше. Эти авторы рассмотрели щель, в которой кристалл с плотно упакованной кубической решет - й разупорядочивается при плавлении вследствие взаимного оттал-вания соприкасающихся атомов. Было рассчитано изменение энтро-ш, сопровождающее каждую из трех стадий плавления. [4]
Поэтому непосредственно за плавлением кристаллов благородных газов происходит их испарение. [5]
Минимумы на кривой соответствуют кристаллам благородных газов, образованным за счет слабых сил межмолекулярного взаимодействия. В больших периодах для s - и / - элементов ( главные подгруппы) эта закономерность также просматривается. Однако на нее накладывается изменение энтальпий в рядах переходных металлов. [6]
ГЦК и ГПУ упаковки характерны для элементов с почти сферической симметрией межатомных связей кристаллов благородных газов, многих металлов. [7]
Молекулярные кристаллы, с которы-ми мы достаточно кратко здесь познакомились, представляют собой за исключением кристаллов благородных газов типичный пример так называемых гетеродесмичвских систем. Что означает это слово. Heteros с греческого переводится, как иной, отличный; desmos - связь. Следовательно, гетеродесмический кристалл - это кристалл, в котором одновременно имеются несколько различных типов связи между атомами. [8]
Молекулярные кристаллы образуют органические, металло-органщеские, многие комплексные соединения, а также бинарные соединения типа Н2О, СО2, НС1 и др. В форме молекулярных кристаллов могут находиться некоторые твердые простые вещества: Н2, галогены ( С12, Br2, I2), N2, O2, Sg. Кристаллы благородных газов ( элементов с полностью заполненными электронными оболочками: Не, Ne, Ar, Кг, Хе, Rn) хотя и построены из атомов, но относятся к молекулярным, так как связи между атомами в них имеют ван-дер-ваальсовый характер. Молекулярные кристаллы делятся на гомомолекулярные, состоящие из одинаковых молекул, и гетеромолекулярные, состоящие из разных молекул. [9]
Ван-дер-ваальсовы силы слабые ( меньше кулонов-ских), короткодействующие, центральные. Типичными представителями веществ являются кристаллы благородных газов и вследствие того, что силы связи малы, эти кристаллы существуют при очень низких температурах. Силы Ван-дер - Ваальса типичны для некоторых анизотропных кристаллов, образующихся из элементов IV - VII групп ( см. рис. 3, б) по правилу 8 - N. В них между атомными слоями ( рядами, молекулами) действуют силы Ван-дер - Ваальса, а между атомами внутри слоев ( рядов, молекул) ковалентные связи. [10]
С некоторой осторожностью следует пренебрегать тройными взаимодействиями, когда речь идет о сравнении энергий нескольких возможных кристаллических структур определенного вещества. Так, для всех кристаллов благородных газов, кроме Не, потенциалы Леннард-Джонса предсказывают гексагональную плотную упаковку при 0 К как самую выгодную энергетически, тогда как на самом деле благородные газы кристаллизуются в гранецентрированную решетку. [11]
 |
Зависимость энтальпии атомизации гомоатомных соединений от порядкового номера элементов. [12] |
Это обусловлено, с одной стороны, упрочнением связей в кристаллах по мере увеличения числа валентных электронов от одного до четырех, а с другой - уменьшением прочности кристаллической решетки за счет уменьшения координационного числа ковалентных структур по правилу 8 - N после IVA-группы. Минимумы на кривой соответствуют кристаллам благородных газов, образованным за счет слабых сил межмолекулярного взаимодействия. В больших периодах для s - и р-элементов ( главные подгруппы) эта закономерность также просматривается. Однако на нее накладывается изменение энтальпий в рядах переходных металлов. При этом для металлов первой вставной декады, обладающих кайносимметрич-ными 3 / - электронами, наблюдается четко выраженная внутренняя периодичность, обусловленная особой стабильностью ( / 5 - и f - конфигурации и меньшей способностью электронов в этом состоянии к валентному взаимодействию. Именно по этой причине кристаллические структуры марганца ( 3P4s2) и цинка ( 3i104s2) менее прочны. Эта тенденция менее ярко выражена у остальных ( / - элементов, особенно в середине вставных декад, где более явно проявляется горизонтальная аналогия. Тем не менее, для простых веществ, замыкающих rf - ряды ( Cd, Hg), отмечаются минимумы энтальпии атомизации. [13]
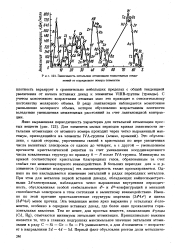 |
Зависимость энтальпии атомизации гомоатомных соединений от порядкового номера элементов. [14] |
Это обусловлено, с одной стороны, упрочнением связей в кристаллах по мере увеличения числа валентных электронов от одного до четырех, а с другой - уменьшением прочности кристаллической решетки за счет уменьшения координационного числа ковалентных структур по правилу 8 - N после IVA-группы. Минимумы на кривой соответствуют кристаллам благородных газов, образованным за счет слабых сил межмолекулярного взаимодействия. В больших периодах для s - и р-элементов ( главные подгруппы) эта закономерность также просматривается. Однако на нее накладывается изменение энтальпий в рядах переходных металлов. При этом для металлов первой вставной декады, обладающих кайносимметрич ными ЗЛ-электронами, наблюдается четко выраженная внутренняя периодичность, обусловленная особой стабильностью Р - и ( / - конфигураций и меньшей способностью электронов в этом состояний к валентному взаимодействию. Именно по этой причине кристаллические структуры марганца ( 3.4 s2) и цинка ( 3P 4s2) менее прочны. Эта тенденция менее ярко выражена у остальных rf - эле-ментов, особенно в середине вставных декад, где более явно проявляется горизонтальная аналогия. Тем не менее, для простых веществ, замыкающих rf - ряды ( Cd, Rg), отмечаются минимумы энтальпии атомизации. [15]
Страницы: 1 2 3