Массовая доля - элемент
Cтраница 3
Стех - В примере, приведенном выше, стехиометрическая смесь состоит из одного моля СЩ и двух молей кислорода 02, что соответствует массе элемента кислорода О 64 г и полной массе 80 г. Поэтому массовая доля элемента Zo. [31]
Условное обозначение проволоки состоит: из индекса Нп ( наплавочная); следующих за индексом Нп после дефиса цифр, указывающих на среднюю массовую долю углерода в сотых долях процента; цифр после буквенных обозначений химических элементов, указывающих среднюю массовую долю элемента в процентах. Буква А указывает на повышенную чистоту металла проволоки по содержанию серы и фосфора. После состава в обозначении проволоки приводят номер стандарта. [32]
К первой группе относятся вычисления по формулам химических соединений: вычисление относительной молекулярной ( и молярной) массы соединения по его формуле; вычисление массы элемента в определенном количестве вещества; вычисление массы вещества, содержащей определенное количество элемента; вычисление массовой доли элемента в молекуле. [33]
Для экспериментального определения молярных масс эквивалента химических элементов используют: 1) прямой метод, основанный на данных по синтезу водородных или кислородных соединений элемента; 2) косвенный метод, в котором вместо водорода и кислорода используют другие элементы с известным эквивалентом; 3) метод вытеснения водорода из кислоты металлом взятой навески; 4) аналитический метод, основанный на определении массовой доли элемента в одном из его соединений; 5) электрохимический метод, использующий данные электролиза. Если для элемента известны значения степени окисления и Аг, то молярная масса эквивалента может быть вычислена из отношения первой величины ко второй. [34]
Их обозначают буквами Бр, элементы сплава - по аналогии с латунями, дополнительно используя следующие буквы: Ф - фосфор; Б - бериллий; Т - титан; Мг - магний; Кд - кадмий; X - хром. Цифры указывают среднюю массовую долю элементов сплава ( %) в том же порядке, что и буквы; остальное - средняя массовая доля меди. Буквы, обозначающие элементы сплава, в деформируемых бронзах указываются подряд ( далее следуют соответствующие цифры через дефис), в литейных - указываются по порядку буквы и цифры. [35]
Значения Л /, Ьк и а к представлены в табл. 6 как усредненные для всего объема имеющейся отечественной и зарубежной информации. Сведения, относящиеся к измерениям малых массовых долей элементов в экспериментах отдельных стран ( например, [7]) в большинстве случаев недостаточны для надежной оценки параметров линии регрессии а - с. Это делает преждевременными выводы о существенных различиях в качестве измерений в тех или иных экспериментальных массивах. [36]
В некоторых задачах по выводу формул горючих веществ ( чаще всего - органических) вместо массовых долей элементов приводятся данные о массах ( количествах, объемах) продуктов сгорания. На основании этих данных достаточно просто рассчитываются массовые доли элементов или число молей атомов в сгоревшем веществе. [37]
В обозначении марок стали первые две цифры указывают среднюю массовую долю углерода в сотых долях процента, буквы за цифрами означают: Г - марганец, С - кремний, X - хром, Ф - ванадий, В - вольфрам, Н - никель. Цифры, стоящие после букв, указывают примерную массовую долю элемента в целых единицах. Отсутствие цифры означает, что в марке содержится до 1 5 % этого легирующего элемента. В наименовании марок стали, с массовой долей до 0 9 % марганца ( по верхнему пределу), буква Г не ставится. [38]
Изучая § 1.4, вы уже познакомились с тем, как рассчитываются массовые доли элементов в сложных веществах по формулам этих веществ. Однако в химической практике нередко возникает и обратная задача - установление формулы вещества по массовым долям элементов, входящих в его состав. Прежде чем рассматривать методику решения задач такого типа, следует познакомиться с понятием эмпирическая формула вещества. Все те формулы веществ, с которыми вы встречались при изучении предыдущих параграфов, называются молекулярными формулами. Например, молекулярная формула глюкозы С6НиО6 показывает, что одна молекула ее состоит из 6 атомов углерода, 12 атомов водорода и 6 атомов кислорода. [39]
Химик, определяющий атомную массу нового элемента X в середине XIX в. Он получил четыре соединения А, Б, В, Г, содержащие элемент X, и определил массовую долю элемента в каждом из них. [40]
Химическая реакция соответствует движению реагентов вдоль траектории в ( 2 П5) - размерном фазовом пространстве состояний, в котором находятся также энтальпия, давление и массовые доли ns компонентов. Стартуя с различных начальных условий, реагирующая система развивается, пока не достигнет точки равновесия. При этом химическое равновесие зависит только от энтальпии h, давления р и массовых долей элементов Zj ( см. гл. [41]
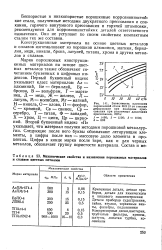 |
Механические свойства и назначение порошковых материалов и сплавов цветных металлов. [42] |
Марки порошковых конструкционных материалов на основе цветных металлов также обозначают сочетанием буквенных и цифровых индексов. Первый буквенный индекс указывает класс материалов: Ал - алюминий, Бе - бериллий, Бр - бронза, В - вольфрам, Г - марганец, Д - медь, Ж - железо, Л - латунь, М - молибден, Мг - магний, Н - никель, О - олово, П - фосфор, С - кремний, Св - свинец, Ср - серебро, Т - титан, Ф - ванадий, X - хром, Ц - цинк, Цр - цирконий. Второй буквенный индекс П указывает, что материал получен методами порошковой металлургии. Следующие после него буквы обозначают легирующие элементы, а цифры после них - массовую долю элемента в процентах. Цифра в конце марки после тире, как и для черных металлов, обозначает группу пористости материала. [43]
С точки зрения атомно-молекулярного учения в процессе образования молекулы обычно участвует небольшое число атомов, которые соединяются всегда в строго определенном количественном соотношении. Поэтому количественный состав образующихся молекул, а следовательно, и состав образующихся веществ молекулярного строения оказывается постоянным. В процессах же образования кристаллов немолекулярного ( атомного или ионного) строения участвует очень большое число частиц, которые соединяются не всегда в строго определенном количественном соотношении. Поэтому количественный состав образующихся атомных или ионных кристаллов может быть переменным в зависимости от способов их получения. Количественный состав сложных веществ удобно выражать через массовые доли элементов. [44]
Страницы: 1 2 3