Молекулярный кристалл
Cтраница 2
Молекулярные кристаллы, помимо инертных газов, встречаются у элементов V, VI, VII групп. За исключением металлического полония и полуметаллических сурьмы и висмута, в этих элементах атомы связаны ковалентными силами в молекулы, которые в свою очередь связаны ван-дер-ваальсовыми силами. В итоге связь оказывается смешанной, ковалентно-молекулярной. [16]
 |
Кристаллическая структура алмаза. [17] |
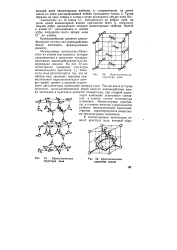
Молекулярные кристаллы образуются из атомов или молекул, которые удерживаются в кристалле вандерва-альсовыми взаимодействиями или водородными связями. На рис. 50 для иллюстрации приведена структура молекулярного кристалла 12 - Молекулы иода располагаются так, что их центры масс занимают вершины прямоугольного параллелепипеда и центры граней, причем в решетке существуют две различные ориентации молекул иода. Так же как и в случае жидкости, полуколичественной мерой энергии взаимодействия между частицами в кристалле является температура, при которой происходит изменение агрегатного состояния, в данном случае температура плавления. [18]
 |
Кристаллическая структура алмаза.| Кристаллическая структура диоксида кремния. [19] |
Молекулярные кристаллы, образуются из атомов или молекул, которые удерживаются в кристалле ван-дер-ваальсовыми взаимодействиями или водородными связями. Молекулы иода располагаются так, что их центры масс занимают вершины прямоугольного параллелепипеда и центры граней, причем в решетке существуют две различные ориентации молекул иода. Как и в случае жидкости, полуколичественной мерой энергии взаимодействия между частицами в кристалле является температура, при которой происходит изменение агрегатного состояния, в данном случае температура плавления. Молекулярные кристаллы, в которых частицы удерживаются слабыми нековалентными взаимодействиями, характеризуются невысокими температурами плавления. [20]
Молекулярные кристаллы образуют органические, металло-органщеские, многие комплексные соединения, а также бинарные соединения типа Н2О, СО2, НС1 и др. В форме молекулярных кристаллов могут находиться некоторые твердые простые вещества: Н2, галогены ( С12, Br2, I2), N2, O2, Sg. Кристаллы благородных газов ( элементов с полностью заполненными электронными оболочками: Не, Ne, Ar, Кг, Хе, Rn) хотя и построены из атомов, но относятся к молекулярным, так как связи между атомами в них имеют ван-дер-ваальсовый характер. Молекулярные кристаллы делятся на гомомолекулярные, состоящие из одинаковых молекул, и гетеромолекулярные, состоящие из разных молекул. [21]
Молекулярный кристалл состоит из димеров ( АВ) 2, однако расположение молекул АВ неизвестно. [22]
 |
Растворимость s иодида натрия ( NaJ в г на 100 г растворителя в различных растворителях при 25 С. [23] |
Молекулярные кристаллы хорошо растворимы ( табл. 14), но выбор растворителя зависит от природы молекул вещества, в первую очередь, от их полярности и способности к установлению Н - свя-зей. Это соответствует старому эмпирическому правилу: подобное растворяется в подобном. Это значит, что вещества, состоящие из полярных молекул, лучше растворяются в полярных растворителях, чем в неполярных, и наоборот. [24]
Молекулярные кристаллы хорошо растворимы ( табл. 14), но выбор растворителя зависит от природы молекул вещества, в первую очередь, от их полярности и способности к установлению Н - связей. Это соответствует старому эмпирическому правилу: подобное растворяется в подобном. Это значит, что вещества, состоящие из полярных молекул, лучше растворяются в полярных растворителях, чем в неполярных, и наоборот. [25]
Молекулярные кристаллы - Вг2, 12, СН4, нафталин, парафин, многие твердые органические соединения. В узлах кристаллических решеток таких кристаллов находятся молекулы, сохранившие свою индивидуальность. Между этими молекулами действуют силы притяжения, характерные для взаимодействия молекул ( II. Относительно малая устойчивость молекулярных кристаллов, низкие температуры плавления объясняются тем, что силы притяжения между их молекулами меньше, чем у кристаллов других типов. [26]
 |
Кристаллическая структура графита.| Цепочечная структура кристаллов карбина. [27] |
Молекулярные кристаллы представляют собой молекулы, соединенные силами межмолекулярного взаимодействия, включая и другие дополнительные виды связей ( см. с. [28]
Молекулярные кристаллы также представляют обширные возможности для изучения влияния состава жидкой среды на понижение прочности твердого тела. Так, для неполярных веществ, например твердых углеводородов, наибольшие эффекты понижения прочности проявляются под действием жидких неполярных сред, тогда как по мере увеличения полярности среды происходит повышение межфазной энергии и ослабление эффектов уменьшения прочности. Это иллюстрируется рис. XI-28, на котором в координатах, отвечающих уравнению Гриффитса, сопоставлены отношения прочностей чистых образцов нафталина РО и - в ПРИСУТСТВИИ СреДЫ РА И Соответствующих значений межфазной энергии 00 и ад; поверхностная энергия определялась расщеплением монокристаллов нафталина по методу Обреимова - Гилма-на ( см. § 4 гл. [29]
Молекулярные кристаллы - Вг2, 12, СН, нафталин, парафин, многие твердые органические соединения. В узлах кристаллических решеток таких кристаллов находятся молекулы, сохранившие свою индивидуальность. [30]
Страницы: 1 2 3 4