Кристаллизация - сульфат - кальций
Cтраница 3
Из приведенных данных видно, что кристаллизация сульфата кальция представляет собой сложный процесс. Его кинетика зависит не только от обычных параметров, таких как пересыщение, температура, состав раствора и перемешивание. Она усложнена возможностью кристаллизации метастабильных фаз и фазовыми превращениями кристаллогидратов друг в друга. Поэтому кристаллизация CaSO4 в условиях получения фосфорной кислоты должна описываться уравнениями, учитывающими особенности ярко выраженного гетерогенного процесса а также одновременное течение процессов растворения и кристаллизации. [31]
Кремневая кислота, наоборот, способствует кристаллизации сульфата кальция в виде тонких игл. [32]
Нлстокшее исследование является продолжением работы по кристаллизации сульфатов кальция из жидкостей дистилляции в отсутствии затраг-ки безводного сульфата кальция и ставит своеЛ целью полнее гзучить кинетику фазовых переходов двугидрата в полугидрат и измене. Изиестно, что кригые растворимостей двугидрата и полугидрата в воде и растворах пересекаются с изменением температуры и существует взаимная обратимость. Есть основание ожидать иной зависимости продолжительности существования метаста-бильлого двугилргта от концентрации 5ОГ в исходной смеси растворов, чем F. [33]
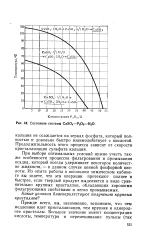 |
Состояние системы CaSCu-PtOs - Н2О. [34] |
Продолжительность этого процесса зависит от скорости кристаллизации сульфата кальция. [35]
Аналогичное действие оказывают растворимые фосфаты и на кристаллизацию сульфата кальция. [36]
Торможение разложения фосфата кислотой может быть обусловлено кристаллизацией сульфата кальция на поверхности зерен фосфата непосредственно из диффузионного пограничного слоя 91 - 93 и замедлением вследствие этого диффузии ионов Са2 в массу раствора. Наблюдениями под микроскопом найдено8, что эффект пассивирования зерен фосфата определяется размерами и формой образующихся кристаллов сульфата кальция. При высоких концентрациях серной кислоты ( выше 63 %) жидкая фаза быстро пересыщается сульфатом кальция, вследствие чего выделяется большое количество мелких ( длиной 5 - 7 мк и шириной I-2 мк кристаллов CaSO4 0 5H2O и CaSO4 в форме иголочек, образующих налеты, которые покрывают почти всю поверхность зерен апатита. Это затормаживает реакцию, в результате чего процесс протекает недостаточно полно и суперфосфатная масса с недостаточным количеством сульфата кальция плохо схватывается. Содержащаяся в ней жидкая фаза остается на поверхности твердых частиц и получается не рассыпчатый, а мажущий продукт с плохими физическими свойствами. Они не покрывают поверхность зерен фосфата сплошным слоем, а образуют пористую рыхлую корку, в меньшей степени затрудняющую диффузию кислоты к зернам. Поэтому реакция идет быстро и получается сухой рассыпчатый продукт, так как остающаяся жидкая фаза впитывается в поры между кристаллами. [37]
Имеются схемы с разделением стадий растворения апатита и кристаллизации сульфата кальция, а также при одновременном осуществлении этих стадий. [38]
При температурах испарения выше 110 - 115 С кристаллизация сульфата кальция не может быть предотвращена никакой продувкой. [39]
В этих условиях скорость разложения фосфата мала, кристаллизация сульфата кальция протекает медленно и, вследствие большой вязкости кислоты, отделение ее от осадка весьма затруднительно. [40]
В этих условиях скорость разложения фосфата мала, кристаллизация сульфата кальция протекает медленно и, вследствие-большой вязкости кислоты, отделение ее от осадка весьма затруднительно. [41]
Основные направления и принципы совершенствования процессов растворения фосфатов и кристаллизации сульфата кальция рассмотрены ниже. Они детально обсуждены также в ряде других работ [29, 67], подтверждены результатами опытных исследований и практикой их широкого промышленного использования. [42]
Изучению скорости растворения фосфатов в сернофосфорно-кислых растворах на фоне кристаллизации сульфата кальция посвящено незначительное число работ. Это объясняется отсутствием простых и надежных методик и трудоемкостью исследования. В одной из немногих работ [27], выполненных для условий процесса получения экстракционной фосфорной кислоты из фосфоритов Флориды, показано, что скорость растворения этих фосфоритов при 65 - 85 С в растворах фосфорной кислоты, содержащих 25 - 35 % Р2О5 и до 1 5 % H2SO4, такова, что в течение 1 - 15 мин обеспечивается практически полное растворение фосфата. [43]
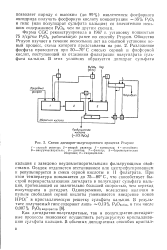 |
Схема дигидрат-полугидратного процесса Ргауоп. [44] |
Как дигидратно-полугидратные, так и полугидратно-дигидрат-ные процессы позволяют осуществить регулируемую кристаллизацию сульфата кальция. [45]
Страницы: 1 2 3 4