Совместная кристаллизация
Cтраница 1
Совместная кристаллизация обеспечивает установление связей как внутри кристаллов, так и по границам зерен. [1]
Совместная кристаллизация различных металлов не ограничивается всегда только образованием смешанных кристаллов, как это уже упоминалось на стр. В ряде случаев при определенных атомных соотношениях возможно возникновение новых структур. [2]
Совместную кристаллизацию изотопов свинца и кадмия с кристаллами хлористого натрия Бус [6] объясняет специфической адсорбцией ионов свинца и кадмия на определенных плоскостях растущего кристалла. [3]
Исследована совместная кристаллизация азотнокислого калия и двухромового калия из растворов при различных температурах и исходных концентрациях. Установлено, что характер кристаллизации бихромата калия определяется его исходной концентрацией в жидкой фазе. [4]
При совместной кристаллизации из неполярной среды форма кристаллов остается орторомбической, а их размер зависит от содержания циклических углеводородов в смеси с ал-канами, и чем больше циклических углеводородов, тем меньше размер кристаллов и меньше число наслоений. [5]
При совместной кристаллизации церезинов и парафинов из раствора в неполярных растворителях повидимому имеют место два явления. Первое заключается в том, что при охлаждении раствора первичными зародышевыми кристаллами являются кристаллы церезина. При дальнейшем понижении температуры раствора начинают кристаллизоваться парафины, которые вследствие присущей им полимерфности кристаллизуются в форме церезинов, и поэтому мы получаем кристаллическую структуру смеси параф-и-ков и церезинов, аналогичную церезиновой. [6]
При совместной кристаллизации из углеводородных сред форма кристаллов остается орторомбической, а их размер зависит от содержания циклических углеводородов в смеси с парафинами, и чем больше концентрация таких углеводородов в смеси, тем меньше размер кристаллов. Такую же форму имеют и смешанные кристаллы парафиновых и циклических углеводородов ( рис. 49, г, д), причем чем больше в смеси нафтеновых и особенно ароматических углеводородов, тем меньше размер кристаллов и больше их усеченность. Кристаллическая структура твердых углеводородов изменяется в присутствии смолистых веществ. [7]
При совместной кристаллизации двух или более веществ они могут в некоторых случаях образовать общую кристаллическую решетку. [8]
Кривая совместной кристаллизации начинается на стороне AgCl - КС) при 318 и оканчивается при 440 - 450 внутри тройной системы. [9]
При совместной кристаллизации двух или более веществ они могут в некоторых случаях образовать общую кристаллическую решетку. [10]
При совместной кристаллизации из расплава получается сплав эвтектического состава 2 0 мол. [11]
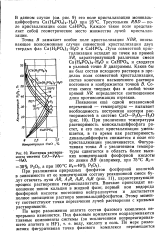 |
Изотермы растворимости системы СаО - PjOs. [12] |
Лучи совместной кристаллизации исходят из точек на прямой NR, характеризующей различные смеси Са ( Н2РО4) 2 - Н2О и СаНРО4, и сходятся в узловой точке В диаграммы. Каков бы ни был состав исходного раствора в пределах поля совместной кристаллизации, состав конечного насыщенного раствора постоянен и изображается точкой В. Состав смеси твердых фаз в любой точке прямой NR определяется соотношением длин противолежащих отрезков. [13]
Линия совместной кристаллизации BaSO4 и ВаС12 имеет спад температур от 826 до 786 С. [14]
Линии совместной кристаллизации, разделяющие поля непрерывных твердых растворов, имеют незначительные минимумы. [15]
Страницы: 1 2 3 4