Возбужденный атом - бор
Cтраница 1
Возбужденный атом бора имеет три неспаренных электрона - один s - и два р-электрона. [1]
В возбужденном атоме бора имеется один 25-электрон и два электрона на 2 / о-орбитали. А возбужденный углерод характеризуется одним s - электроном и тремя неспаренными р-электронами ( см. гл. Однако в соединениях бора и углерода ( например, ВС13, СН4, ССЦ и др.), соответственно все три и четыре связи эквивалентны. [2]
 |
Схема sp - гибридизации [ IMAGE ] Линейная молекула ВеС1з. [3] |
В возбужденном атоме бора имеются один 2в - электрон и два электрона на двух 2р - орбиталях. А возбужденный атом углерода характеризуется одним s - электро-ном и тремя неспаренными р-электронами. Однако в соединениях бора и углерода ( например, ВС1з, СЩ, СС14 и др.) соответственно все три или четыре связи эквивалентны. [4]
 |
Схема гибридизации [ IMAGE ] Линейная молекула. [5] |
В возбужденном атоме бора имеются один 2-электрон и два электрона на двух 2р - орбиталях. А возбужденный атом углерода характеризуется одним - электроном и тремя неспаренными р-электронами. [6]
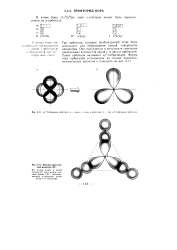 |
Плоская треугольная молекула BFj. [7] |
Три орбиталн, которые возбужденный атом бора использует для образования связей, совершенно одинаковы. Они получаются в результате смешения электронных плотностей одной s - и двух р-орбиталей. [8]
 |
Строение молекулы 32. [9] |
При взаимодействии одного S - и двух Р - облаков образуются три гибридных электронных облака, ч го имеет место например, в атоме бора. Возбужденный атом бора имеет три неспаренных электрона. [10]
Гибридизация одной s и двух р-орбиталей ( s р2 - г и б р и д и з а ц и я) имеет место при образовании соединений бора. Как уже указывалось, возбужденный атом бора обладает тремя неспаренными электронами - одним s - электроном и двумя р-электронами. Из трех орбиталей образуются три эквивалентные. Действительно, как показывают экспериментальные исследования, молекулы таких соединений бора, как ВГ3 ( Г - - галоген), В ( СН3) 3 - триметилбор, В ( ОН) 3 - борная кислота, имеют плоское строение. При этом три связи бора в указанных молекулах имеют одинаковую длину и расположены под углом 120 друг к другу. [11]
Как уже указывалось, возбужденный атом бора обладает тремя неспаренными электронами - одним s - электроном и двумя р-электронами. Действительно, как показывают экспериментальные исследования, молекулы таких соединений бора-как ВГ3 ( Г - галоген), В ( СН3) з - триметилбор, В ( ОН) 3 - борная кислота, имеют плоское строение. [12]
 |
Пространственное расположение гибридных орбиталей атома углерода. [13] |
Такая гибридизация имеет место при образовании соединений бора. Как уже указывалось, возбужденный атом бора имеет три неспаренных электрона - один s - электрон и два р-электрона. [14]
 |
Схема связей в молекулеС2. [15] |
Страницы: 1 2