Кристаллогидрат - сульфат - медь
Cтраница 3
Попутно с получением меди на лекции показать, как получается безводный сульфат меди. Грубоизмельченный кристаллогидрат сульфата меди CuSO4 - 5H2O осторожно нагревать в маленькой фарфоровой чашке, помешивая стеклянной палочкой до тех пор, пжа не образуется белый порошок. [31]
Состав кристаллогидратов принято изображать формулами, показывающими, какое количество кристаллизационной воды содержит кристаллогидрат. Например, кристаллогидрат сульфата меди ( медный купорос), содержащий на один моль CuS04 пять молей воды, изображается формулой CuSO4 бЩО; кристаллогидрат сульфата натрия ( глауберова соль) - формулой Na2SC4 ЮЩО. [32]
Некоторые кристаллогидраты при нагревании до определенной температуры теряют только воду, а разложение вещества происходит при более высокой температуре. В частности, кристаллогидрат сульфата меди теряет полностью кристаллизационную воду при температуре 258 С, превращаясь в безводную соль; разложение безводного сульфата меди начинается при 653 С. [33]
Здесь ковалентная связь также образована по донорно-акцепторному механизму: двухэлектронные облака атомов кислорода ( донора) принимаются ионом меди ( акцептором) и становятся общими. Поэтому правильно было бы формулу кристаллогидрата сульфата меди изображать как [ Cu ( H2O) 4 ] SO4 - H O. Однако по традиции формулы кристаллогидратов изображают иначе ( например, CuSO4 - 5H2O), помня, что это сложное ( комплексное) соединение ( см. гл. [34]
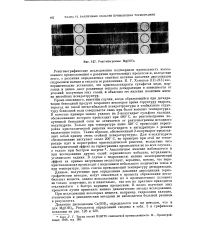 |
Рентгенограммы Mg ( OH a. [35] |
III-213 ] экспериментально установил, что кристаллогидраты сульфатов меди, марганца и цинка дают различные теплоты дегидратации в зависимости от условий получения этих солей, и объяснил это явление наличием именно нестойких псевдоструктур. [36]
Присоединяя к себе воду, сульфат меди образует синие кристаллы. Кристаллогидрат сульфата меди CuS04 - 5H20 называется медным купоросом. Водные растворы сульфата меди имеют синий цвет. Такие гидратированные ионы содержатся и в самом кристаллогидрате. По этой же причине и растворы ряда других солей двухвалентной меди, например, Cu ( N03) 2, CuCl: 2 и др., также имеют синий цвет. [37]
Она входит в состав различных сплавов ( с. Широко применяются соединения меди. Например, кристаллогидрат сульфата меди ( II) ( медный купорос) CuSO SHzO необходим для борьбы с вредителями и болезнями растений. [38]
Кристаллогидраты - это вещества, кристаллизующиеся с одной или несколькими молекулами воды. Некоторые кристаллогидраты при нагревании до определенной температуры теряют только воду, а разложение вещества происходит при более высокой температуре. В частности, кристаллогидрат сульфата меди теряет полностью кристаллизационную воду при температуре 258 С, превращаясь в безводную соль; разложение безводного сульфата меди начинается при 653 С. [39]
Некоторые кристаллогидраты при нагревании до определенной температуры теряют только воду, а разложение вещества происходит при более высокой температуре. В частности, кристаллогидрат сульфата меди теряет полностью кристаллизационную воду при температуре 220 С, превращаясь в безводную соль; разложение безводного сульфата меди начинается при 653 С. [40]
Некоторые кристаллогидраты при нагревании до определенной температуры теряют только воду, а разложение вещества происходит при более высокой температуре. В частности, кристаллогидрат сульфата меди теряет полностью кристаллизационную воду при температуре 258 С, превращаясь в безводную соль; разложение безводного сульфата меди начинается при 653 С. [41]
Кристаллогидраты - это кристаллические вещества, содержащие так называемую кристаллизационную воду. Многие кристаллогидраты при нагревании до определенной температуры только теряют воду, а разложение самой соли происходит при более высокой температуре. Разложение безводной соли начинается при температуре выше 650 С. Поэтому для-определения формулы кристаллогидрата сульфата меди прокаливание следует вести в интервале 260 - 300 С. [42]
Страницы: 1 2 3