Описанная диаграмма
Cтраница 1
Описанная диаграмма может быть обобщена для продуктов сгорания произвольного. [1]
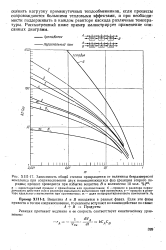
Описанная диаграмма получена при определенной температуре и определенном давлении, которые выбраны таким образом, что парообразная фаза отсутствует. При изменении условий существования системы положения ветвей AM и ВМ и точки М смещаются. Зависимость растворимости солей АХ и Л У от температуры наглядно показывает объемная диаграмма ( рис. 86), по третьей оси координат которой откладывается температура. Объемная диаграмма рис. 86 получается для некоторого постоянного давления. [2]
Описанная диаграмма замечательна тем, что в ней, можно сказать, каждый элемент находит свое надлежащее место. Первый из них - типичный инертный газ, очень сходный с гелием, неоном и другими инертными газами. Второй - столь же типичный щелочной металл, сходный с натрием. На прямой в описанной выше диаграмме каждый элемент оказывается помещенным на том месте, которое соответствует его основным свойствам - кобальт перед никелем и теллур перед иодом. [3]
Описанная диаграмма получена при определенной температуре и определенном давлении, которые выбраны таким образом, что парообразная фаза отсутствует. При изменении условий существования системы положение ветвей AM, BM и точки М сметается. [4]
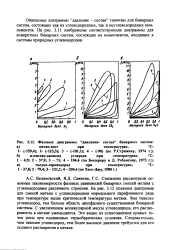 |
Фазовые диаграммы давление - состав бинарных систем. [5] |
Описанные диаграммы давление - состав типичны для бинарных систем, состоящих как из углеводородных, так и неуглеводородных компонентов. На рис. 3.11 изображены соответствующие диаграммы для конкретных бинарных систем, состоящих из компонентов, входящих в системы природных углеводородов. [6]
Описанная диаграмма замечательна тем, что в ней, можно сказать, каждый элемент находит свое надлежащее место. Первый из них - типичный инертный газ, очень сходный с гел-ием, неоном и другими инертными газами. Второй - столь же типичный щелочной металл, сходный с натрием. На прямой в описанной выше диаграмме каждый элемент оказывается помещенным на том месте, которое соответствует его основным свойствам - кобальт перед никелем и теллур перед иодом. [7]
Описанная диаграмма может быть использована для расчета циклического процесса получения соды и нашатыря на базе твердого бикарбоната аммония. Такой процесс выгоднее обычного аммиачно-содового процесса, так как при этом достигается более полная утилизация хлористого натрия, но он может быть осуществлен в широком масштабе только при наличии массового потребления твердого нашатыря. [8]
Описанная диаграмма получена при определенной температуре и определенном давлении, которые выбраны таким образом, что парообразная фаза отсутствует. При изменении условий существования системы положения ветвей AM и ВМ и точки М смещаются. Зависимость растворимости солей АХ и AY от температуры наглядно показывает объемная диаграмма ( рис. 86), по третьей оси координат которой откладывается температура. Объемная диаграмма рис. 86 получается для некоторого постоянного давления. [9]
 |
Прибор, заменяющий построение диаграммы. [10] |
Хотя описанная диаграмма предназначена для машин с неявновы-раженными полюсами, но ее очень часто применяют и к машинам с явновыраженными полюсами. [11]
В описанной диаграмме рассмотрен случай, когда В растворяется в А, давая кр. Такая растворимость называется односторонней. Кроме того, в рассмотренном случае с повышением температуры растворимость увеличивается. [12]
 |
Принцип построения изотермической диаграммы растворимости четвертого типа для простых четырехкомпонентных систем в форме незамкнутого прямого двугранного угла. [13] |
Из этого следует, что описанная диаграмма не может иметь практического применения для графических расчетов, так как ее возможности еще более ограничены, чем в случае диаграммы второго и третьего типов. В действительности этот тип диаграммы в технологических расчетах не используется. [14]
Страницы: 1 2