Критерий - равновесность
Cтраница 1
Критерий равновесности характеризует степень приближения системы к равновесному состоянию. Отношение Н / w характеризует время контакта взаимодействующих фаз. [1]
Рап, Раж - критерии равновесности ( завершенности процесса) для паровой и жидкой фаз. [2]
Определяющий критерий ( Sp ерКрт) отличается от критерия равновесности Q, полученного Дьяконовым, лишь тем, что в на-щем случае в этот критерий входят безразмерная степень суммарного превращения бр, объемная скорость подачи сырья Vp и время контакта т, тогда как критерий Q, по определению самого автора, характеризует меру отношения внутренних скоростей превращения и связь между концентрациями исходных и конечных продуктов превращения. Иными словами, критерий Q является отношением произведений констант скоростей и констант равновесия обратной и прямой реакции, имеющей определенный механизм, выраженный также определенными ( постулированными) стехио-метрическими коэффициентами и компонентами системы. [3]
По физическому смыслу критерии типа ыВ1 / ыв, являются критериями термодинамической равновесности Ра, а критерии типа И / ЫБ, 1 / Ко - кинетическими критериями. Отсюда следует, что для стационарного процесса критерий контакта является мерой отношения скорости обусловливающих процессов обмена к внутренней скорости самого превращения. При в, и, иВг / иВ1 - - 1 процесс приближается к равновесному. Уравнение ( 7) становится безусловно инвариантным. [4]
Поэтому критерий подобия Ра иногда называют также и критерием квазистатичности, хотя другие его названия ( критерий равновесности, обратимости) более четко определяют его содержание. [5]
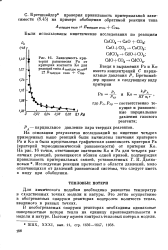 |
Зависимость критерия равновесия Ра от критерия контакта Ко для реакций типа Л твердое. [6] |
На основании результатов исследований по кинетике четырех приведенных выше реакций были вычислены значения критериев Ра и Ко и была представлена графическая зависимость критерия Ра ( критерий термодинамической равновесности) от критерия Ко. Исследуемые реакции протекают в области давлений, мало отличающихся от давлений равновесной системы, что следует иметь в виду при обобщении. [7]
Обоснованная форма выражения функции, характеризующей полноту протекания процессов в массообменных аппаратах, принята в трудах [206, 240, 241] в виде критерия Ра In 1 / ( 1 - TJ), названного [85] критерием равновесности. [8]
Энтропия возрастает, если в системе протекают необратимые процессы. В термодинамике соотношение (1.32) используют как критерий равновесности или неравновесности системы. Для адиабатически изолированной системы при равновесии энтропия достигает максимума. [9]
Направление самопроизвольно протекающих процессов является одним из критериев равновесности фазового состояния полимера. По данным Каргина и Михайлова 132, ориентированное гидратцеллюлозное волокно полностью дезориентируется при кипячении в воде. На основании этого факта был сделан вывод, что состоянию истинного равновесия в целлюлозных материалах отвечает не высокоориентированная структура, а дезориентированное расположение макромолекул. Однако этот вывод недостаточно обоснован. Не говоря уже о том, что по данным тех же авторов при кипячении в течение 10 - 12 ч вискозного или медноам-миачного шелка, сформованного с большой вытяжкой, степень ориентации не понижается 133 и что известны факты повышения ориентации гидратцеллюлозного волокна при прогреве его в глицерине при 200 - 250 С, необходимо учесть, что выбор указанных объектов исследования для ответа на вопрос о равновесном фазовом состоянии целлюлозы не вполне удачен, так как гидратцел-люлозные волокна различной степени ориентации находятся, по-видимому, в одном и том же фазовом состоянии. [10]
Равновесие между исходными реагентами и продуктами химической реакции, происходящей в одной из фаз, определяется константой равновесия / Ср, / Сс или KN так же, как и для гомогенных процессов. При расчете и моделировании гетерогенных процессов степень приближения к равновесию характеризуется критерием равновесности Ра ( см. стр. [11]
Вопросами применения теории подобия для исследования процессов, протекающих с участием химических реакций, занимались Дамкелер, Эджеворт-Джонстон, Траустель. К - Дьяконова [6], который предложил ввести в качестве критериев, характеризующих ход процессов с участием химических реакций, критерий контакта Ко и критерий термодинамической равновесности Ра наряду с обычными гидродинамическими критериями и критериями обмена. [12]
Диффузионный процесс ведет к уменьшению перепада активностей свободного комплексона, при этом эффект сопряженности должен уменьшаться, а значение потенциала электрода, следовательно, во времени должно возрастать. Действительно, при многочисленных повторных калибровках нами было замечено, что изменение потенциала для мембран со средними концентрациями валиномицина, хотя и совместимые с нашими критериями равновесности, носят направленный характер, о связи с этим мы изменили методику исследования и стали фиксировать значения потенциалов электродов в течение суток в каждом из последующих растворов с интервалом в несколько минут в начале опыта к несколько часов в конце. [13]
Если энергия, расходуемая на приращение длины трещины, больше высвобождаемой при этом энергии упругой деформации, то трещина развиваться не может из-за нехватки энергии для этого процесса. Если же Д ( / 27 А /, то трещина развивается самопроизвольно. Таким образом, условие (8.90) есть критерий равновесности трещины. [14]
Если энергия, расходуемая на приращение длины трещины, больше высвобождаемой при этом энергии упругой деформации, то трещина развиваться не может из-за нехватки энергии для этого процесса. Если же AU 2 уЛ /, то трещина развивается самопроизвольно. Таким образом, условие (8.90) есть критерий равновесности трещины. [15]
Страницы: 1 2