Краевой атом
Cтраница 1
Высокоэнергетичныс краевые атомы связаны между собой хр2 - связями и могут активно хемосорбировать кислород. Поверхностные атомы базисных плоскостей, образующие структуру идеальной решетки графита, взаимодействуют за счет наиболее слабых а-связей и обладают значительно меньшей поверхностной активностью. Кроме этого, на поверхности волокна могут быть обнаружены фибриллярная микроструктура, микропоры, границы кристаллитов, посторонние включения, трещины, являющиеся зародышами разрушения. [1]
Насыщение краевых атомов углерода допускается в этом случае при маловероятном наличии большого количества тройных связей. При этом некоторая часть краевых атомов неизбежно останется ненасыщенной. Это связывают с критическим характером температуры в 700, при которой многие исследователи наблюдали резкие изменения свойств коксуемого материала. [2]
По-видимому, прочность связи краевых атомов углерода со своими соседями в базисных плоскостях кристаллитов для обоих типов структур одинакова. [3]
Взаимодействие молекулы кислорода с краевым атомом углерода, входящим в состав ароматического углеродного кольца, удерживаемого двумя скомпенсированными валентными связями при гибридизации, начинается с хемосорбции и образования углерод-кислородного комплекса между третьей нескомпенсиро-ваоной атомной орбиталыо атома углерода и одной из вакантных орбиталей молекулы кислорода. [4]
Несколько прочнее связаны с кристаллом краевые атомы. В зависимости от их расположения и числа связей с атомами соседних слоев они могут иметь различную степень ненасыщенности и, следовательно, разную адсорбционную и реакционную способность. [5]
 |
Схема строения элементарной структурной единицы ( плоскости кристаллита угля, прогретого до 700. [6] |
Здесь видно, что большинство краевых атомов углерода остаются ненасыщенными. Максимальное число таких атомов будет получаться при группировке шестиугольных колец в линию, а минимальное - при круговом расположении последних, образующих цилиндрическую форму отдельного кристаллита. [7]
В результате разрушения углеродных слоев растет доля краевых атомов с ненасыщенными валентностями, и графит становится пирофорным. [8]
С началом аморфизации после 10-часового размола возрастает доля краевых атомов и, как предположили выше, отдельные кристаллиты сшиваются своими краевыми атомами или через неупорядоченный углерод в замкнутые полимерные образования. [9]
По-видимому, углеродные элементы аморфной части срастаются своими краевыми атомами или через неупорядоченный углерод в сажеобразные полимерные образования, которые гомогенно не графитируются. [10]
Одновременно протекает сшивание отдельных кристаллитов и слоев своими краевыми атомами или через неупорядоченный углерод в замкнутые сажеобразные образования. Это компенсирует увеличение свободной энергии, и теплоемкость уменьшается. Такая коагуляция, с другой стороны, приводит к уменьшению скорости роста удельной поверхности и уменьшению плотности. [11]
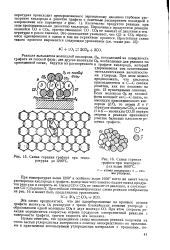 |
Схема горения графита при температурах до 1200 С.| Схема горения графита при температурах выше 1600 С. [12] |
Эта схема предполагает, что две адсорбированные на краевых атомах графита молекулы Оз реагируют с тремя ближайшими атомами углерода с образованием одной молекулы СОа и двух молекул СО. При этом скорость реакции определяется скоростью отрыва продуктов поверхностной реакции с поверхности графита, причем скорость эта невелика. [13]
Можно предположить, что причиной, определяющей возникновение этих носителей тока, являются краевые атомы разорванных боковых цепочек углерода и углеродных слоев, на которых в значительной мере локализуются я-электроны. [14]
С другой стороны, можно предположить, что реакция углерод - двуокись углерода идет на краевых атомах углерода, содержащих два неспаренных электрона; таким образом, эти реагирующие места могут быть блокированы как за счет хемосорбции окиси углерода, так и за счет хемосорбции водорода. Если торможение в реакции углерод - водяной пар имеет место в результате восстановления комплекса поверхность - кислород, окись углерода, так же как водород, должна ингибировать реакцию. Вывод сводится к тому, что торможение как в реакции углерод - водяной пар, так и в реакции углерод - двуокись углерода происходит из-за хемосорбции. [15]
Страницы: 1 2 3 4