Атома-акцептор
Cтраница 1
Стремление атома-акцептора к увеличению своего координационного числа от двух или трех до четырех и более достаточно-велико, и в отсутствие подходящих донорных молекул простые соединения этих элементов могут димеризоваться. Типичным примером является соединение А1С13, которое в растворе и при низкой температуре в газовой фазе является димером ( А12С16) с мости-ковыми атомами хлора; в твердом состоянии оно ассоциировано еще больше: каждый атом алюминия имеет октаэдрическое окружение с тремя парами Костиковых атомов хлора. В структурах-такого типа мостиковые атомы галогенов отдают неподеленные пары электронов, что приводит к образованию обычных двух-электронных связей. Значительно труднее объяснить образование связей в таких димерах, как диборан В2Н6 и алкилы алюминия Al2Re, поскольку в этих молекулах недостаточно электронов для того, чтобы между атомами существовали двухэлектронные связи. [1]
Связи дативного типа понижают вблизи центрального атома-акцептора электронную плотность, возросшую за счет образования донорно-акцепторных связей и, таким образом, способствуют упрочению последних. [2]
В зависимости от химической природы атома-акцептора водородные связи отличаются друг от друга степенью прочности. [3]
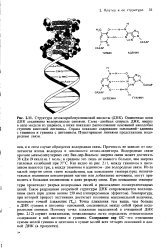
Прочность ее зависит от кислотности атома водорода и основности атома-акцептора. Водородные связи прочнее межмолекулярных сил Ван-дер - Ваалъса: энергия связи может достигать 38 кДж ( 9 ккал) на 1 моль; в среднем это лишь не намного больше, чем энергия тепловых колебаний при 37 С. Как видно из рис. 2.11, между гуанином и цито-зином имеются три, а между тимином и аденином-две водородные связи. Из-за малой энергии связи такие воздействия, как повышение температуры, незначительные изменения концентрации магния или добавление мочевины, могут приводить к большим изменениям и даже разрыву связи. При повышении температуры происходит разрыв водородных связей и расхождение полинуклеотидных цепей. Точка плавления тем выше, чем больше в ДНК гуанина и цитозина-оснований, соединенных между собой тремя водородными связями. Поэтому точка плавления выделенной и очищенной ДНК ( рис. 2.12) служит показателем, позволяющим легко определить относительное содержание в ней цитозина и гуанина. [5]
Образование водородной связи заключается во взаимодействии протона группы ХН с электронной оболочкой атома-акцептора протона и возмущении электронных оболочек атомов X и Y. Это взаимодействие сказывается особенно отчетливо на изменении волнового числа v и интенсивности / полосы группы ХН. На этой группе, ввиду локального характера водородной связи и отсутствия у протона внутренней электронной оболочки, влияние окружения сказывается меньше, чем на других группах, и потому особенности водородной связи могут наблюдаться в более чистом виде. [6]
В таких случаях, когда после образования ковалентной связи только что обобщенные электроны лежат на стороне атома-акцептора от средней точки между двумя атомами, очевидно, произошло окисление. Так обстоит дело при превращении сульфита в сульфат, однако при превращении аммиака в ион алшония дело обстоит иначе. Следовательно, здесь вопрос о том, богат или беден электронами атом, имеющий необобщенные электронные пары, определяется конечным результатом реакций, в которых участвуют именно эти пары электронов. [7]
Положительному решению этого вопроса препятствует также ограниченность сведений о природе и прочности связи в комплексных соединениях между ионами металла и координируемыми лигандами. Среди таких факторов важное значение имеет заряд атома-акцептора, природа атома-донора, самого комплекса и иона, с которым комплекс соединяется. [8]
При этом изменение константы расщепления особенно велико при переходе от апротонных к протонным растворителям, так как сольватация радикалов обусловлена, очевидно, преимущественно водородными связями между растворителем и функциональными группами радикала. Перераспределение спиновой плотности можно объяснить тем, что электроотрицательность атома-акцептора водородного мостика, обладающего неподеленной парой электронов, зависит от растворителя. [9]
Было показано, что на основе такого представления может быть истолковано множество комплексов, если только принять, что присоединяющиеся к центральному атому одновалентные кислотные остатки предоставляют ему только один электрон, в то время как насыщенная в обычном смысле, способная к самостоятельному существованию нейтральная молекула затрачивает по два электрона на неполярную связь. Так как при подобном сочетании происходит некоторый сдвиг центра тяжести отрицательных зарядов в сторону атома-акцептора, то последний должен приобрести избыток отрицательного заряда, в то время как донор должен становиться положительнее. [10]
Было показано, что на основе такого представления может быть истолковано множество комплексов, если только принять, что присоединяющиеся к центральному атому одновалентные кислотные остатки предоставляют ему только один электрон, в то время как насыщенная в обычном смысле, способная к самостоятельному существованию нейтральная молекула затрачивает по два электрона на неполярную связь. Так как при подобном сочетании происходит некоторый сдвиг центра тяжести отрицательных зарядов в сторону атома-акцептора, то последний должен приобрести избыток отрицательного заряда, в то время как донор должен становиться положительнее. [11]
Повышению стабильности гош - конформаций способствует также внутримолекулярная водородная связь. Очевидно, что для образования водородной связи необходима пространственная сближенность водородного атома, обладающего кислыми свойствами, в группе-доноре - X - Н и атома-акцептора Y, который содержит неподеленную пару электронов. В противоположность распространенному неправильному мнению нахождение X, Н и Y на одной прямой не является необходимым для образования водородной связи. Для этиленхлоргид-рина СН2ОНСН2С1 оценка различия энергетических уровней двух возможных конформации была произведена на основании температурной зависимости соотношения интенсивностей частот колебаний свободной и связанной гидроксильных групп [59] ( см. разд. Как оказалось, гога-конформация на 0 95 ккал / молъ более устойчива, чем акяш-конформация. [12]
Страницы: 1