Энергетическая диаграмма - реакция
Cтраница 1
Энергетическая диаграмма реакции приведена на рис. 10, а. Верхняя кривая передает ход некаталитической реакции, нижняя - двухстадийной каталитической. [1]
Энергетическая диаграмма реакции с учетом сольватации приведена на рис. 11, где es - истинная теплота активации, е - теплота активации в отсутствие сольватации, Ца - теплота сольватации активированного комплекса. [2]
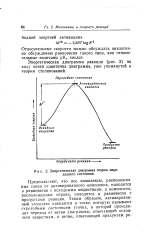 |
Энергетическая диаграмма теории переходного состояния. [3] |
Энергетическая диаграмма реакции ( рис. 2) по виду почти идентична Диаграмме, уже упомянутой в теории столкновений. [4]
Энергетическая диаграмма реакции El на рис. 13.5 показана на примере элиминирования mpem - бутилбромида. [5]
Энергетическая диаграмма реакции нуклеофильного присоединения к карбонильному соединению представлена на рис. 19.2. Переходное состояние в большинстве реакций нуклеофильного присоединения ближе по строению к аддукту, чем к исходному карбонильному соединению. [6]
Пользуясь энергетической диаграммой реакции ( рис. 7 и 8), определим связь между изменением энтальпии и энергиями активации прямой и обратной реакций. [7]
 |
Энергетическая диаграмма реакции с катализатором ( / и без него ( 2. [8] |
На рис. 5.1 изображена энергетическая диаграмма реакции. От аналогичной энергетической диаграммы с участием гомогенного катализатора данная диаграмма отличается теплотами адсорбции и десорбции. [9]
Полезно напомнить, что каждая энергетическая диаграмма реакции соответствует определенной взаимной ориентации в активированном комплексе. Энергетическая диаграмма, которая построена на основе опытных данных, соответствует ориентации, наиболее благоприятной для реакции. Диаграммы с менее благоприятной ориентацией соответствуют большим энергиям активации и меньшим скоростям реакций. [10]
 |
Энергетическая диаграмма стадии развития цепи при хлорировании метана. [11] |
Переходное состояние ( ПС) - максимум на энергетической диаграмме реакции; группа атомов, участвующая в переходном состоянии, называется активированным комплексом. [12]
Оба соединения ацетилируются с существенно различными скоростями. Как видно из энергетической диаграммы реакции ( рис. 5.9), разность между энергиями исходных стереоизомеров составляет около 3 кДж / моль; это та лишняя энергия, которая имеется у цис-изомера вследствие аксиального расположения гидроксильной группы. В ходе ацетилирования образуется переходное состояние; при этом тригональ-ная карбонильная группа ацилирующего агента ( ангидрида или хлор-ангидрида) становится тетраэдрической и связывается с ОН-группой. Объем находящегося в аксиальном положении заместителя существенно возрастает, и тем самым разность энергий переходных состояний оказывается больше разности энергий исходных цис - и транс-изомеров. Иными словами, для достижения переходного состояния цис-изомера надо затратить больше энергии, чем для создания переходного состояния транс-изомера; из этого следует, что превращение ц с-изомера будет происходить с меньшей скоростью. [13]
Предполагаемое гипотетическое состояние, находящееся в термодинамическом равновесии между реагентом и продуктом реакции. Формально максимум на энергетической диаграмме реакции. При этом считается, что химические связи в реагентах еще не разрушены, а связи в продуктах реакции еще не образованы. Переходное состояние существует не дольше одного соударения молекул. [14]
Страницы: 1