Атропизомерия
Cтраница 1
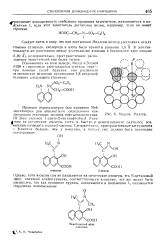 |
Модель Миллса. [1] |
Принцип атропизомерии был применен Мей-зенгеймером для абсолютного определения конфигурации некоторых оксимов нафталинового ряда. [2]
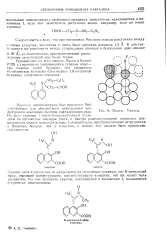 |
Модель Мнллса. [3] |
Принцип атропизомерии был применен Мей-зенгеммеро. [4]
В ряду бифенила такая изомерия называется атропизомерией. Если атропизомеры получены в чистом виде, они показывают оптическую активность ( см. Введ. [5]
 |
Условия для появления атропизомерии. [6] |
Таким образом, условиями, необходимыми для появления атропизомерии производных дифени-ла, являются: 1) невозможность свободного вращения бензольных колец вокруг обшей оси; 2 1 несимметричное замещение каждого кольца. [7]
 |
Условия для появления атропизомерии. [8] |
Таким образом, условиями, необходимыми для появления атропизомерии производных дифени-ла, являются: 1) невозможность свободного вращения бензольных колец вокруг обшей оси; 2) несимметричное замещение каждого кольца. [9]
Приведенный выше пример динафтилового производного показывает, что явление атропизомерии не ограничено дифениловыми системами. [10]
Значения барьеров вращения очень различны. Например, барьер внутреннего вращения этана равен 13 кДж / моль, а для некоторых переходов ( например, для атропизомерии) они столь велики, что внутреннее вращение становится невозможным при комнатной температуре, но легко происходит при повышенной температуре. Вообще с повышением температуры растет код-центрация или, как говорят, заселенность энергетически более богатых конформации. В ряде случаев скорость реакции зависит от энергии перехода обычной конформации в r - конформацию ( высоты барьера между ними) и вероятности этого перехода. Иными словами, скорость реакции зависит от мгновенной концентрации г-кон-формации в веществе. [11]
Страницы: 1