Ксенат
Cтраница 1
Ксенаты образуются при взаимодействии ХеОз с щелочами. Триоксид ксенона ХеОз - белое, нелетучее, чрезвычайно взрывчатое соединение ( ДЯ. [1]
Известны ксенаты, содержащие Xe ( VI), и перксенаты [ производные Xe ( VIII) ], например CsHXe04 синтезирован из ХеОз. CsOH в присутствии ионов F -, а гидратированные соли, содержащие ион Хе054, получены при взаимодействии XeF6 и гндроксидов щелочных металлов. [2]
Как получают ксенаты и перксенаты. [3]
С, его солеобразные производные - ксенаты ( 6) - известны. [4]
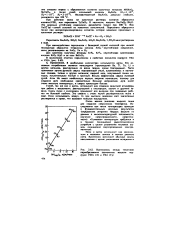 |
Взаимосвязь между теплотами парообразования элементных веществ подгрупп VIIIA О и VIIA ( Гг. [5] |
При действии озона на щелочные растворы ксенатов образуются к сенаты ( VIII), или перксенаты Э ХеОб. Это довольно устойчивое соединение, разлагается только при 300 С. Ион ХеО - р) - самый сильный из известных окислителей. [6]
Соли первой кислоты называют ксенонатамн или ксенатами, а второй - перксенатами. При нагревании до 100 С этот кристаллогидрат обезвоживается, и получается безводная соль, которая устойчива до температур выше 300 С. [7]
Известны соли этой кислоты, например Ва3ХеО3 - ксенат бария. [8]
Хотя сами эти кислоты неустойчивы, их соли - ксенаты ( например, Na4XeOe и Ва3ХеО6) и перксенаты ( например, Na6XeO6, Ba2XeO6) - при комнатной температуре представляют собой достаточно устойчивые кристаллические вещества. [9]
Хотя сами эти кислоты неустойчивы, их соли - ксенаты ( например, Na4XeO6, Ва3ХеО6) и перксенаты ( например Na6XeOe, Ba2XeO6) - при комнатной температуре представляют собой достаточно устойчивые кристаллические вещества. [10]
Хотя сами эти кислоты неустойчивы, их соли - ксенаты ( например, NaeXeO6, Ва3ХеО6) и перксенаты ( например, Na4XeO6, Ba2XeOe) - при комнатной температуре представляют собой достаточно устойчивые кристаллические вещества. [11]
Кристаллическая сода 412 Кристаллогидраты 294 Кристобалит 13, 363 Ксенат бария 504 Ксенон 501 ел. [12]
Триокснд ксенона является кислотным оксидом, ему соответствует, например, соль ксенат ( У1) бария ВаДеОв, представляющая собой малорастворимые белые кристаллы. Ди-хлорид ксенона XeClj - белые кристаллы, устойчивые в отсутствие воды до ЬОСС. [13]
В настоящее время получены оксиды и гидроксиды, например ХеО4, ХеО3, Н2ХеО5, НвХеОв, Н2КгО4 и соли указанных кислот - Na 6ХеО в ( гипоксенат), ВаКЮ4 ( гипокриптат), Na2XeO5 ( ксенат) идр. [14]
Из кислородных соединений, помимо оксида ксенона ( VI) ХеОз, получены оксид ксенона ( VIII) ХеО4, а также соответствующие им кислоты - HeXeOg и Н4ХеОб - Хотя сами эти кислоты неустойчивы, их соли - ксенаты ( например, На4ХеОб, ВазХеОв) и перксенаты ( например NagXeOg, Ba2XeOg) - при комнатной температуре представляют собой достаточно устойчивые кристаллические вещества. [15]
Страницы: 1 2