Ксмплексон
Cтраница 1
Ксмплексоны применяют в качественном анализе главным образом в качестве маскирующих реактивов при открытии катионов обычными неорганическими и специальными органическими реактивами. [1]
В присутствии этилендиаминтетрауксусной кислоты ( ЭДТА, ксмплексона III, трилона Б) могут быть осуществлены следующие разделения. [2]
Аналитики должны обратить внимание еще на одно большое преимущество ксмплексона. [3]
Для амперометрического определения серебра в нейтральном или аммиачном растворе ксмплексона Малинек и Ржехак рекомендуют применять в качестве осаждающего реактива спиртовый раствор меркаптофенилтиотиодиазолона или меркаптобензотиазо-ла. Определение проводят с вращающимся платиновым микроэлектродом, соединенным накоротко меркурйодидным электродом сравнения. [4]
Извлечение бериллия производят из 100 мл раствора, содержащего 2 5 % ксмплексона III и по 2 5 мг каждого из отделяемых элементов. Скорость пропускания раствора через колонку длиной 8 см и диаметром 1 см равна 0 45 мл / мин. Cd, Hg, Pb и Mn не сорбируются диаллилфосфатной смолой в указанных условиях. Уран также поглощается смолой, но может быть десорбирован раствором карбоната натрия. [5]
Данные Флашки использовали Киннунен и Мериканто [57] для разработки улучшенных методов косвенного определения палладия и золота, в которых выделившийся по вышеприведенному уравнению реакции никель связывается ксмплексоном, а избыток последнего обратно титруют солью марганца по эрио-хрому черному Т в качестве металлиндикатора. Метод пригоден для определения палладия или золота в присутствии платины и других драгоценных металлов, так как последние не образуют комплексов с цианидом. [6]
В приведенных случаях хотя константы скорости образования и распада комплекса еще могут быть определены, но их значения так велики, что при смешивании растворов, содержащих ион металла и ксмплексон, происходит практически мгновенное образование комплекса. [7]
Из полученного раствора отбирают пипеткой аликвотные части по о мл, переносят их в две мерные колбы емкостью по 100 мл, прибавляют в каждую по 20 мл воды, 5 мл 0 2 М раствора ксмплексона, 4 мл 0 1 М раствора нитрата кальция, 3 мл 0 5 % - ного раствора желатины, 30 мл концентрированного аммиака и доводят до метки водой. В первую колбу вносят перед доведением до метки стандартный раствор цинка. [8]
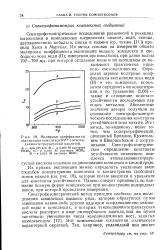 |
Молярные коэффициенты. [9] |
Из кривых экстинкции можно определить указанным выше способом концентрацию комплекса и концентрацию свободных ионов никеля ( см. рис. 18), которые потом вводятся в уравнение для константы устойчивости. Однако следует принимать во внимание ионную форму ксмплексона при концентрации водородных ионов, при которой проводятся измерения. [10]
Присутствие ионов Zn ( NH3) в растворе определяют при соответствующем потенциале полярографически. При этом способе титрования ионы цинка функционируют в качестве амперометрического индикатора. Форма кривой, когда, кроме кальция и цинка, присутствует также магний, отличается лишь тем, что по окончании титрования кальция раствором ксмплексона образуется комплекс не только с цинком, но и частично с магнием. [11]
К слабокислому раствору ванадата прибавляют около 0 5 - 1 0 г сульфита натрия и кипятят до тех пор, пока раствор не окрасится в чисто-синий цвет. Нагревают до кипения, разбавляют охлажденной водой до 200 - 300 мл и после прибавления 0 1 г аскорбиновой кислоты слабо подщелачивают раствор аммиаком и титруют 0 01 М раствором сульфата марганца по эриохрому черному Т до появления винно-краснсй окраски. Переход окраски очень отчетлив. В этом случае титруют вытесненный марганец непосредственно 0 01 М раствором ксмплексона. [12]
Страницы: 1