Медный кулометр
Cтраница 3
В некоторых случаях последовательно с медным включают газовый водородно-кислородный кулометр. Тогда электролиз происходит с выделением меди в медном кулометре и выделением эквивалентного количества гремучего газа в газовом кулометре. [31]
Требуется определить пористость оловянных покрытий в зависимости от их толщины. Для этого необходимо: 1) определить катодный выход олова по току, применяя медный кулометр; 2) пользуясь полученным значением выхода по току, рассчитать время осаждения для получения покрытий заданной толщины ( уравнения для расчета приведены на стр. [32]
Катод кулометра взвешивается дважды: до и после электролиза. Разность весов, равная весу металла, осажденного в: результате прохождения тока, позволяет вычислить по формуле ( 14) величину количества электричества, пропущенного в течение электролиза. Медный кулометр находит широкое применение в электрохимической практике. [33]
Катод кулометра взвешивается дважды: до и после электролиза. Разность весов, равная весу металла, осажденного в результате прохождения тока, позволяет вычислить по формуле ( 14) величину количества электричества, пропущенного в течение электролиза. Медный кулометр находит широкое применение в электрохимической практике. [34]
Через 5 часов после включения тока в электролизер на-ливают при помощи пипетки ( в стеклянную трубку) такое количество крепкой соляной кислоты ( по расчету), чтобы - 1 / з гипохлорита, содержащегося в электролите, перешла в хлорноватистую кислоту. После прибавки кислоты делают еще два газовых анализа ( через 15 мин. Катод медного кулометра вынимают и взвешивают. [35]
Электролизеры, служащие для определения количества электричества, называются кулометрами. Для точной работы куло-метра необходимо, чтобы в нем протекал лишь один электрохимический процесс без каких-либо побочных реакций и чтобы продукты электролиза поддавались точному взвешиванию или измерению. Простейшим и наиболее доступным из них является медный кулометр. [36]
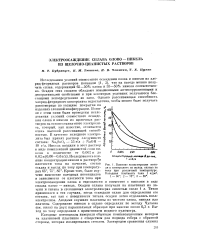 |
Влияние концентрации никеля в электролите на выход сплава по току при различной температуре. Катодная плотность тока 1 а / дм2. 1 - 60. 2 - 75. 3 - 85е. [37] |
Титан применялся в тех случаях, когда осаждали сплав для определения его состава, так как с поверхности титана осадки легко отделялись после электролиза. Анодами служили пластины из чистого олова, никеля или платины. Содержание никеля в сплаве определяли по методу Чугаева ( см. ниже) на двух параллельных образцах при навеске около 0 3 г. Выход по току определяли с применением медного кулометра. [38]
Продолжительность электролиза, в зависимости от выбранной плотности тока, не превышает 45 - 70 минут. Для определения зависимости выхода по току от длительности процесса один из электролизеров выключают по истечении Vs назначенного времени, второй выключают через 2 / з и только последний электролизер работает до конца. При выключении каждого электролизера из него извлекают алюминиевый анод, промывают его и погружают в сосуд с водой. Одновременно извлекают катод медного кулометра и определяют его привес. [39]
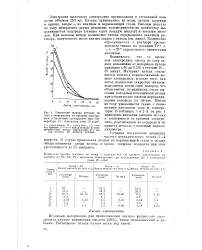 |
Изменение выхода металла по току и зависимости от времени электролиза в щелочном электролите при температуре 20, плотности тока 20 а / дм2. [40] |
Выяснилось, что со временем электролиза выход по току падает независимо от материала катода примерно с 60 до 0 5 % в течение 20 - 30 минут. Материал катода сказывается только в первоначальный момент электролиза, и после того, как катод полностью закроется титаном, выделяется почти один водород, что объясняется, по-видимому, очень высоким катодным потенциалом титана при относительно низком перенапряжении водорода на титане. Выход по току уменьшается также с повышением плотности тока и температуры. В таблицах 1 и 2 и на рис. 1 приведены значения выходов по току в зависимости от времени электролиза, рассчитанные по водороду и по привесу металла с помощью медного кулометра. [41]
В качестве электролизера может служить аккумуляторный сосуд емкостью 150 - 200 мл. В него помещают электроды из рольного свинца толщиной 1 - 1 5 мм. Два анода располагают около стенок сосуда; катод помещают между анодами. Собрав схему ( рис. 17), заполняют электролизер электролитом. Взвешивают катод медного кулометра и включают ток. Силу тока устанавливают, исходя из плотности тока, указанной выше ( стр. [42]
Страницы: 1 2 3