Электрохимический кулонометр
Cтраница 1
Электрохимические кулонометры по своей сущности являются электролизерами, в которых каким-либо способом, определяют количество вещества, образовавшегося после катодной, анодной или суммарной реакции при условии 100 % - ного выхода по току для осуществляемых электродных процессов. После определения количества образовавшегося вещества, пользуясь законом Фарадея, легко вычислить количество электричества Q, если известно уравнение реакции. [1]
Электрохимические кулонометры представляют собой электролизеры, в которых определяют массу продукта, образующегося в растворе или выделяющегося на электроде ( электродах) со 100 % - ной эффективностью. По массе образовавшегося продукта рассчитывают Q. В зависимости от природы реакции и способа определения массы выделившегося продукта электрохимические кулонометры подразделяются на гравиметрические, титрационные, газовые, спектрофотометрические и др. Среди них высокой точностью отличается серебряный кулонометр. Однако он неудобен в работе из-за рыхлости образующегося на катоде осадка частиц серебра, которые осыпаются при промывании электрода. [2]
Для измерения количества электричества используют электрохимические кулонометры. [3]
В практике лабораторных электрохимических измерений электрохимические кулонометры служат для определения выхода по току и для других целей. [4]
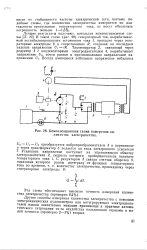 |
Компенсационная схема измерения количества электричества. [5] |
Другие способы измерения количества электричества с помощью электрохимических кулонометров или интегрирующих электродвигателей нашли значительно меньшее применение в практике автоматического титрования из-за неудобства пользования первыми и малой точности ( примерно 2 - 3 %) вторых. [6]
По способу определения количества вещества, образовавшегося в ходе электрохимической реакции, электрохимические кулонометры делятся на несколько групп: электрогравиметрические, титра-ционные, газовые, колориметрические и кулонометрические. [7]
Для определения количества электричества, прошедшего через электролизер при окислении или восстановлении анализируемого вещества, применяются как электронные системы ( интеграторы, логарифмические и специальные двухкоординатные самописцы), так и электрохимические кулонометры: электрогравиметрические ( медные, серебряные, галогено-серебряные); газовые; колориметрические; титрационные; кулонометрические. Кулонометры первого типа основаны на принципе взвешивания катода после осаждения на нем слоя металла. В кулонометрах второго типа измеряется объем образующегося при электролизе газа. Приборы третьего типа основаны на измерении оптической плотности раствора, изменяющейся в ходе электролиза. В кулонометрах четвертого типа образующиеся при электролизе растворимые продукты титруют стандартными растворами. Анодное и катодное пространства в таких приборах разделяются пористыми мембранами во избежание нежелательных химических реакций. [8]
Простейший электрохимический кулонометр позволяет определить суммарное количество электричества, прошедшего в цепи за данное время, либо по увеличению массы катода, включенного последовательно в цепь электролитической ячейки, либо по изменению рН раствора, либо по объему выделившегося газа. Метод требует дополнительных операций и не позволяет считывать результат непосредственно со шкалы прибора. Более совершенными являются приборы с хемотронными преобразователями ( электрохимическими интеграторами), включенными в качестве датчика в электронную измерительную цепочку. [9]
Кулонометры ( интеграторы) обычно бывают трех типов: электрохимические, электромеханические и электронные. Измерение с помощью электрохимических кулонометров основано на взвешивании металлического осадка ( обычно меди или серебра), титровании электрохимически генерируемых частиц, например иода или гидроксид-иона, или измерении объема выделившихся газов. Автор настоящей главы на собственном опыте убедился, что хорошим и простым прибором такого типа является обычный бытовой счетчик постоянного тока, снабженный подходящим шунтом и калиброванный в соответствующем диапазоне тока [44] К сожапению, такие приборы в настоящее время почти не выпускаются промышченностью и нх точность при малых токах ( мене 2 мА) неудовлетворительна В последнем случае можно пользоваться газовым кулоиометром ( для электролиза в небольшом масштабе), но более удобен электронный интегратор, обладающий широким набором рабочих диапазонов тока [379,391] Электронными интеграторами снабжено также большинство потеициостатов. [10]
Электрохимические кулонометры представляют собой электролизеры, в которых определяют массу продукта, образующегося в растворе или выделяющегося на электроде ( электродах) со 100 % - ной эффективностью. По массе образовавшегося продукта рассчитывают Q. В зависимости от природы реакции и способа определения массы выделившегося продукта электрохимические кулонометры подразделяются на гравиметрические, титрационные, газовые, спектрофотометрические и др. Среди них высокой точностью отличается серебряный кулонометр. Однако он неудобен в работе из-за рыхлости образующегося на катоде осадка частиц серебра, которые осыпаются при промывании электрода. [11]
Количество электричества Q, прошедшее через электрическую цепь в виде постоянного тока, измерить довольно просто, так как в этом случае оно представляет собой произведение величины тока на время. Если ток меняется во времени, то количество прошедшего электричества определяют с помощью кулонометров или интегрированием изменяющегося тока по времени. Существуют три основных способа определения количества электричества в цепях постоянного тока: математическое интегрирование, интегрирование тока с использованием интеграторов и измерение с помощью электрохимических кулонометров. Следует заметить, что независимо от типа используемого кулонометра он должен быть включен в схему последовательно с электрохимической ячейкой. [12]
Кулонометры представляют собой особого типа электролизеры. Определение прошедшего через них количества электричества основано на применении закона Фарадея. Электрохимические кулонометры делятся на три класса: 1) весовые, в которых количество электричества определяется по привесу катода вследствие выделения металла из раствора его соли под действием тока; 2) объемные, в которых непосредственно измеряется объем выделившихся в результате электролиза веществ, например объем гремучего газа; 3) титрационные, в которых количество образовавшегося при электролизе вещества определяется его титрованием. [13]
При этом методе в цепь генераторных электродов включают еще одну электролитическую ячейку, в которой генераторный ток вызывает электрохимические процессы, дающие возможность судить о количестве электричества, прошедшего в цепи за время анализа. Результат фиксируют либо по изменению массы, либо по объему выделившегося газа, либо путем проведения обратного электролиза уже при постоянной величине генераторного тока. В последнем случае в качестве источника тока используют схемы с электронной стабилизацией. Электрохимические кулонометры обеспечивают весьма высокую точность измерения ( ошибка менее 0 1 %), однако в автоматизированных приборах их использование едва ли целесообразно. [14]
В ходе кулонометрических измерений необходимо точно определить заряд, проходящий через электрод до появления сигнала конечной точки. Если опыт проводят в гальваностатических условиях ( при постоянной силе тока), заряд определяют как произведение силы тока на точно измеренное время опыта. Если же ток во время опыта непрерывно изменяется, то удобнее использовать специальные кулонометры - счетчики, количества электричества. Электрохимические кулонометры основаны на законах Фарадея; в них измеряют объем выделяющегося газа или ртути, который пропорционален количеству электричества. Существуют также электромеханические кулонометры. [15]
Страницы: 1 2