Лепинь
Cтраница 1
Лепинь [263] дает интерпретацию пассивного состояния металлов, основанную на теории окисных пленок Фарадея, и предполагает, что пассивность металлов вызывается поверхностными соединениями, в особенности кислородными, свойства которых существенно отличаются от свойств продуктов объемно и реакции. Чем меньше расстояние между атомами, тем труднее идут объемные реакции и тем благоприятнее условия для поверхностных реакций. Описывая каталитическую активность металлов при гидрогенизации бензола, Вест-линг [472] расположил металлы по коротким атомным расстояниям в решетке в ряд: никель, кобальт, медь, рутений, родий, иридий, осмий, палладий и платина; он утверждал, что активность металла снижается пропорционально удалению короткого атомного расстояния от обоих пределов. [1]
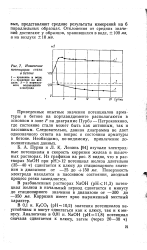 |
Изменение потенциала стали. [2] |
К - Лепинь [94] изучали электродные потенциалы и скорость коррозии железа в щелочных растворах. Из графиков на рис. 8 видно, что в растворах NaOH при рН12 потенциал железа длительно ( 35 - 40 ч) сдвигается к плюсу до стационарного значения в диапазоне от - 25 до 150 мв. Поверхность электрода находится в пассивном состоянии, анодный процесс резко замедляется. [3]
Шилов и Лепинь [45] считали, что участие адсорбента в адсорбционных процессах определяется не только его электрокапиллярными силами, но и его молекулярными силами. Они предполагали, что адсорбент создает определенное поле сил, которое является функцией химических свойств веществ, участвующих в адсорбционном процессе и потому специфических по характеру. Явление адсорбции рассматривалось этими исследователями как равнодействующая комплекса молекулярных сил адсорбента, подвергаемого адсорбции вещества и растворителя. Функция растворителя в процессах адсорбции состоит не только в том, что он частично адсорбируется сам, но также в том, что происходит распределение адсорбируемого вещества между твердой и жидкой фазами. [4]
К - Лепинь и ее сотрудников23 на характер взаимодействия металлов с водой. При взаимодействии мелкораздробленного цинка с водой продуктами реакции являются гидроокись цинка и водород. В промежуточной стадии реакции образуются непрочные соединения-гидриды цинка. Скорость образования конечных продуктов, при разложении которых выделяется водород, зависит от скорости образования и разложения гидрида металла, его свойств и других факторов. [5]
У нас в Советском Союзе накоплен огромный опыт по синтезу неорганических соединений, употребляющихся в качестве препаратов и химических реактивов. Лепинь, Неорганический синтез; В. [6]
 |
Схематический вид кривых коагуляции смесью электролитов. [7] |
Сделано было немало попыток дать теоретическое объяснение явлений антагонизма и сенсибилизации ионов, исходя, главным образом, из адсорбционных свойств коллоидных частиц. К - Лепинь и Бромберга ( 1940 г.), трактующие эти явления с электростатической точки зрения как результат весьма сложного электростатического и химического взаимодействия между ионами. [8]
Такова гипотеза Лэнгмюра, впервые указавшего на хемосорб-цию с образованием, в зависимости от химической природы К и А, двухмерных пленок, валентно связанных с К, по всем участкам поверхности ( см. гл. К этим гипотезам примыкают модели образования поверхностных соединений Лепинь [56], Ридила [57], Пшежецкого [58] и других авторов, а также представления об образовании твердых растворов. [9]
Кинетика таких реакций носит топохимический характер. Лепинь с сотрудниками по взаимодействию коллоидальных аллюминия и цинка с водой 0 - 4 ] Однако, в большинстве опубликованных работ по взаимодействию металлов с водой топокинетические закономерности для описания таких процессов не привлекались, а кинетика реакций лантаноидов с водой и вовсе не изучена. [10]
По существу гипотезы отличались друг от друга разными характеристиками промежуточных форм, в том числе связей К с А. Такова гипотеза Лэнгмюра, впервые указавшего а хемосорб-цию с образованием, в зависимости от химической природы К и А, двухмерных пленок, валентно связанных с К, по всем участкам поверхности ( см. гл. К этим гипотезам примыкают модели образования поверхностных соединений Лепинь [56], Ридила [57], Пшежецкого [58] и других авторов, а также представления об образовании твердых растворов. [11]
Тонкая и интересная гипотеза Н. Е. Веденеевой, близкая к концепции образования поверхностных хелатов, во многих случаях химической обработки не может, однако, достаточно убедительно объяснить различные эффекты при взаимодействии красителей и глины. Концепция поверхностно-химических соединений носит более общий характер и применима для широкого круга органических и неорганических веществ. При поверхностно-химических реакциях адсорбирующиеся молекулы образуют химические соединения, которые, однако, не выделяются в виде новой фазы и сохраняют связь с кристаллической решеткой, на которой они образовались. Лепинь считает такого рода продукты промежуточными, стехиометрически и фазово неопределенными. Келли указывает, что при благоприятных условиях, например повышенной температуре, поверхностная реакция может перейти в объемный процесс хемосорбции. [12]
С этой точки зрения становятся понятными и данные Адлера и Штейгмана. Поэтому область рН, изученную авторами этой работы, следует разбить на две: до рН 4, где иХг находится в ионной форме, и после рН 4, где иХг переходит в коллоидное состояние. Интересно отметить, что образование максимумов на кривых адсорбция-время наблюдалось только в сильнокислых средах. В нейтральных растворах адсорбция UXX на угле плавно возрастала со временем, не образуя максимума. Шилов и Лепинь [ 2В1 ] и Каргин с сотрудниками [252 -285 ] отмечали, что вытесняющее действие электролитов при молекулярной адсорбции зависит от свойств молекул этих соединений, а не только от свойств составляющих их ионов. [13]
Однако в отсутствие кислорода разрушение значительно меньше, чем можно было бы ожидать. При недостатке кислорода коррозионный процесс значительно замедляется. В производственных условиях было показано, что многие ингибиторы, которые в отсутствие кислорода весьма эффективны при малых дозировках, в присутствии сколь-либо заметных количеств кислорода становятся относительно мало эффективными даже при высоких дозировках. В отсутствие окислителя пленка гидроокиси железа очень плотно прилегает к стальной поверхности и, в конечном счете, оказывает защитное действие. Пурин и Лепинь [35] детально рассмотрели это явление, указав, что в первоначальном катодном процессе участвует кислород, но по мере уменьшения его содержания вблизи металла механизм изменяется. Поверхностные пленки тогда эффективно замедляют коррозию. Эти пленки образуются при электрофоретической миграции положительно заряженных коллоидных частиц - РеО ( ОН) к катодным участкам и разряде их. При повышении содержания соли растворимость кислорода понижается. К тому же вследствие более высоких зарядов коллоидных частиц улучшается сцепление их осадков с поверхностью металла. [14]
С этой точки зрения становятся понятными и данные Адлера и Штейгмана. UXt может адсорбироваться на угле не только в коллоидной, но и в молекулярной форме. Поэтому область рН, изученную авторами этой работы, следует разбить на две: до рН 4, где 11Хг находится в ионной форме, и после рН 4, где иХх переходит в коллоидное состояние. Интересно отметить, что образование максимумов на кривых адсорбция-время наблюдалось только в сильнокислых средах. В нейтральных растворах адсорбция UX1 на угле плавно возрастала со временем, не образуя максимума. Шилов и Лепинь [118] и Каргин с сотрудниками р16 119 ] отмечали, что вытесняющее действие электролитов при молекулярной адсорбции зависит от свойств молекул этих соединений, а не только от свойств составляющих их ионов. [15]
Страницы: 1