Лимитирование - процесс
Cтраница 2
Важнейшим свойством эмульсий является их устойчивость. При анализе устойчивости дисперсных систем обычно исходят из предположения лимитирования процесса стабилизации или адсорбцией молекул ( частиц) стабилизаторов, или отталкиванием адсорбционных слоев. [16]
Важнейшим свойством эмульсий является их устойчивость. При анализе устойчивости дисперсных систем обычно исходят из предположения лимитирования процесса стабилизации или адсорбцией молекул ( частиц) стабилизаторов, или, отталкиванием адсорбционных слоев. Рассмотрим факторы, определяющие стабильность эмульсий, исходя из обеих предпосылок. Чтобы не подпустить капли на расстояние, при котором происходит коалесцен-ция, молекулы или частицы стабилизатора должны иметь определенное строение, а также прочно и с плотной упаковкой располагаться на поверхности. [17]
В построенных зависимостях есть одна тонкость: в самом начале процесса, когда ря 1 или хв 0, наблюдаемая скорость превращения WK стремится к бесконечности. Это можно объяснить малой толщиной слоя инертной прослойки, что делает предположение лимитирования процесса массопереносом через него мало обоснованным, и модель внутридиффузионного режима [ см. уравнение (4.41) ] становится не применима. Следовательно, полученный результат WH - при хв - 0 - это свойство уравнений, а не процесса, поскольку эти уравнения перестают быть моделью последнего. [18]
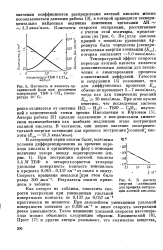 |
Плотность и вязкость органической фазы при различном содержании ТБФ в СС14 ( температура 20 С.| К расчету энергии., активации для процесса экстракции азотной кислоты. [19] |
По ] углу наклона прямой с помощью уравнения Ар-рениуса была определена [ экспериментальная энергия активации ( Еоп), которая составляет - 1 0 ккал / молъ. Температурный эффект скорости перехода азотной кислоты является дополнительным доводом для заключения о лимитировании процесса конвективной диффузией. [20]
Другими словами, если есть сомнение при выборе теории ( быстрой или мгновенной реакции), следует выбрать такую теорию, которая предсказывает более низкую скорость абсорбции. Это обусловлено тем, что при г - оо теория быстрой реакции, которая не учитывает возможность лимитирования процесса стадией диффузии жидкого реагента, предсказывает бесконечную скорость абсорбции, в то время как в действительности скорость абсорбции имеет верхний предел, обусловленный конечной скоростью диффузии жидкого реагента. [21]
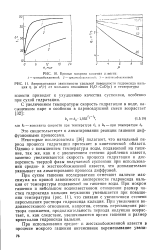 |
Кривые мокрого гашения извести.| Аппроксимация зависимости удельной поверхности гидроксида кальция т ] ( в м2 / г от мольного отношения H2O. CaO ( ij и температуры. [22] |
Некоторые исследователи [36] полагают, что начальный период процесса гидратации протекает в кинетической области. Однако с повышением температуры воды, подаваемой на гашение, так же, как и с увеличением степени дробления извести, заметно увеличиваются скорость процесса гидратации и дисперсность твердой фазы получаемой суспензии при использовании средне - и жесткообожженной извести, что дополнительно указывает на лимитирование процесса диффузией. [23]
Скорость потока растворенных веществ, может контролироваться диффузией через мембрану или диффузией через пленку жидкости, примыкающую к мембране. Пленочная диффузия является лимитирующей стадией в тех случаях, когда коэффициенты диффузии через мембрану высоки ( или когда мембрана очень тонка); плохое перемешивание приводит к получению толстых пленок и в том случае, когда существует небольшое различие между концентрацией агентов в растворе и мембране. Вследствие этого лимитирование процесса пленочной диффузией проявляется наиболее часто в случае противоионов. [24]
При образовании в процессе выщелачивания плотной оболочки твердого продукта наибольшую величину обычно имеет сопротивление l / ffo и процесс, лимитируемый диффузией через этот слой, протекает во внутренней диффузионной области. Если такая оболочка не образуется ( 1 / 20) и величина k достаточно велика, процесс может происходить во внешней диффузионной области при лимитировании его скорости диффузией через слой раствора. В случае же лимитирования процесса скоростью химической реакции он протекает в кинетической области. [25]
Скорость растворения арсенида галлия также в основном определяется скоростью химической реакции на поверхности монокристалла с энергией активации около 12 ккал / моль. В отличие от германия и арсенида галлия растворение антимонида галлия происходит с более низкими значениями энергии активации и возрастает в перемешиваемом растворе по сравнению с неподвижным. Величина пэ Ж - Приведенные данные свидетельствуют о лимитировании процесса растворения GaSb диффузией в растворе. [26]
Но и при неизменной гидродинамике величина / См изменяется по ходу процесса, поскольку величина / п в уравнении (19.10) зависит от состава. Считать Км константой можно лишь в двух случаях: в пределах действия закона Генри и, когда один из членов правой части уравнения (19.10) мал по сравнению с другим. Этот случай соответствует лимитированию процесса массоотдачей в одной из фаз. [27]
Соответствующая ситуация представлена на рис. 5.18: переход от R к Xj тормозится. Применительно к поверхности катализатора это означает, что число центров адсорбции СО ( адс) и О ( адс) начинает лимитировать процесс. Подобная картина обычно наблюдается в том случае, когда при температурах, соответствующих высоким скоростям реакции, уменьшается давление. В этой ситуации процесс лимитируется массопереносом, поскольку число молекул, соударяющихся с поверхностью катализатора в единицу времени, уменьшается. Необходимо обратить внимание, что лимитирование массопереносом отличается от лимитирования процесса адсорбцией в-обычных условиях протекания реакции. [28]
Скорость реакции, отнесенная к единице массы катализатора, зависит не только от порозности, но и от концентрации реагентов и температуры. В этом случае зависимость может оказаться значительно более сложной, чем при некаталитических реакциях. Чтобы имело место явление катализа, реагенты должны продифундировать через поры. При этом скорость процесса может лимитироваться реакцией или диффузией, либо та и другая стадия будут оказывать на скорость процесса почти одинаковое воздействие. Если скорость лимитируется реакцией, что типично для низких температур, то влияние концентрации и температуры будет таким же, как и при химической реакции. Наоборот, если скорость лимитируется диффузией, что типично для более высоких температур, то влияние концентрации и температуры аналогично влиянию, имеющему место при диффузии. В переходной области, в которой на общую скорость процесса влияют как реакция, так и диффузия, эффект температуры и концентрации на процесс часто оказывается довольно сложным. Как следует из предыдущего изложения, определяющим фактором2 является относительная величина константы скорости k и коэффициент диффузии D или точнее отношение D / x, где х - расстояние, на котором осуществляется диффузия. Если D / x велико по сравнению с k, что соответствует лимитированию процесса химической реакцией, то реагенты будут легко диффундировать ко всем частям внутренней поверхности катализатора. В этом случае скорость реакции, отнесенная к единице массы, будет пропорциональна общей поверхности ( внутренней и внешней) и будет экспоненциально зависеть от температуры. В противоположном случае, когда k больше D / x, значительная часть внутренней поверхности будет неактивной ( поскольку реагент не в состоянии ее достичь) и в пределе, когда D / x пренебрежимо мало, реакция локализуется на внешней поверхности. [29]
Страницы: 1 2