Линия - постоянная концентрация
Cтраница 2
Стороны квадрата, расположенные горизонтально, представляют собой линии постоянных концентраций ( 100 и 0 %) анионов, а вертикальные стороны квадрата - линии постоянных концентраций ( 100 и 0 %) катионов. [16]
Поскольку нормируемые величины ПДК не зависят от скорости и направления ветра, значения этих концентраций целесообразно наносить на схему в виде окружностей с центром в точечном источнике, если он незатененный ( Я 2 5 Язд), в виде линий постоянных концентраций от заветренной стены здания, если точечный источник затененный ( Я С2 5 Язд), и в виде прямых линий, параллельных заветренным стенам здания, если источник линейный. Такая план-схема с нанесенными линиями изоконцент-раций даст возможность быстро определить участки с высокой степенью загрязнения воздушного пространства на территории предприятия и в районе жилой застройки и выявить источники выброса, создающие сверхнормативные загрязнения. Разумеется, составлению планов-схем должны предшествовать измерения валовых количеств загрязняющих веществ и соответствующие расчеты ( см. гл. [17]
Графически система ТЮ2 - H2S04 - ( NH4) 2S04 - H20 изображалась по методу Иенеке. Линии постоянной концентрации воды ( изогидры) построены приближенным методом, по криволинейным разрезам. [18]
Диаграммы энтропия-температура ( s - Т) и энтропия-энтальпия ( s - i) схематически изображены на рис. 244, где нанесены пограничные кривые аммиака и воды и изобары р0 и р паровой и жидкой фаз. Каждая пара линий постоянных концентраций промежуточного значения этой величины между 0 и 1 изображает пограничные кривые такого раствора. Например, линии постоянной концентрации 0 5 жидкой и паровой фаз являются пограничными кривыми рабочего тела. Таким образом, энтропийные диаграммы раствора по существу представляют собой сетку пограничных кривых, расположенных между линиями чистого аммиака и воды. Каждая пара этих кривых дает основу для своей полной энтропийной диаграммы. Нанесение всего множества таких диаграмм на один лист затруднительно, поэтому в полных текстах диаграмм автор ограничился только пограничными кривыми для некоторых значений концентраций. Для более полной характеристики состояния рабочего тела в диаграммах нанесены изобары жидкой и паровой фаз, представляющих собой геометрическое место точек одного и того же давления на различных пограничных кривых. [19]
 |
К расчету непрерывной противоточной абсорбции летучим абсорбентом. [20] |
Поскольку числитель и знаменатель в ( с), как видно из ( п) и ( р), одинаковы для любого сечения абсорбера, то и х - некоторая постоянная для всех сечений аппарата концентрация ПК. В поле треугольной диаграммы линии постоянных концентраций ( х const) параллельны стороне ГН - А треугольника. Характерная для конкретного аппарата линия х const может быть расположена как выше, так и ниже стороны ГН - А. [21]
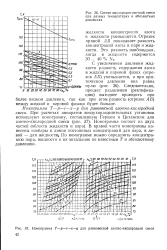 |
Состав кислородно-азотной смеси при разных температурах и абсолютных давлениях.| Номограмма Т - р - i-х-у для равновесной азотно-кислородной смеси 42. [22] |
В правой части номограммы нанесены изобары и линии постоянных концентраций для пара, в левой - для жидкости. [23]
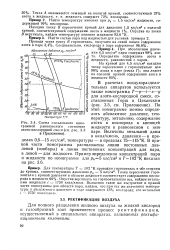 |
Схема пользования номограммой равновесного состояния азото-кислородной смеси ( в Приложении. [24] |
Величины энтальпий даны в ккал / кмоль, давления - в пределах 0 5 - 15 кгс / см2, температуры - в пределах 75 - 115 К. В правой части номограммы расположены линии постоянных давлений ( изобары) и линии постоянных концентраций для пара, в левой - для жидкости. [25]
В правой части номограммы расположены линии постоянных давлений ( изобары) и линии постоянных концентраций для пара, в левой-для жидкости. [26]
Зависимость процесса энергетических превращений от пространственной структуры р есть проявление тонкого механизма развития неустойчивости, при котором возмущение должно соответствующим образом организоваться, чтобы заимствовать доступную кинетическую и потенциальную энергию у основного течения. Заметим, что каждый раз, когда возмущения приобретают энергию, ориентация изолиний ф оказывается в точности противоположной ориентации линий постоянной концентрации пассивной примеси ( таких, как полосы краски), отклоняемых сдвиговым течением. [27]
Диаграммы энтропия-температура ( s - Т) и энтропия-энтальпия ( s - i) схематически изображены на рис. 244, где нанесены пограничные кривые аммиака и воды и изобары р0 и р паровой и жидкой фаз. Каждая пара линий постоянных концентраций промежуточного значения этой величины между 0 и 1 изображает пограничные кривые такого раствора. Например, линии постоянной концентрации 0 5 жидкой и паровой фаз являются пограничными кривыми рабочего тела. Таким образом, энтропийные диаграммы раствора по существу представляют собой сетку пограничных кривых, расположенных между линиями чистого аммиака и воды. Каждая пара этих кривых дает основу для своей полной энтропийной диаграммы. Нанесение всего множества таких диаграмм на один лист затруднительно, поэтому в полных текстах диаграмм автор ограничился только пограничными кривыми для некоторых значений концентраций. Для более полной характеристики состояния рабочего тела в диаграммах нанесены изобары жидкой и паровой фаз, представляющих собой геометрическое место точек одного и того же давления на различных пограничных кривых. [28]
Величины энтальпий даны в ккал / кмоль, давления-в пределах 0 5 - 15 кгс / см2, температуры-в пределах 75 - 115 ЭК. В правой части номограммы расположены линии постоянных давлений ( изобары) и линии постоянных концентраций для пара, в левой-для жидкости. [29]
Величины энтальпий даны в ккал / кмоль, давления-в пределах 0 5 - 15 кгс / см2, температуры-в пределах 75 - 115 К. В правой части номограммы расположены линии постоянных давлений ( изобары) и линии постоянных концентраций для пара, в левой-для жидкости. [30]
Страницы: 1 2 3