Линия - нейтральность
Cтраница 3
Образующаяся при титровании соль - ацетат натрия - дает при гидролизе слабощелочную среду, и поэтому точка эквивалентности не совпадает с линией нейтральности. Следовательно, для данного случая можно применить индикатор фенолфталеин, рТ которого равен 9 0 и входит в область скачка. [31]
Графическая зависимость, вычисленная по уравнению (3.20) для разных рКкисл и рКосн, приведены на рис. 3.1. В верхней части диаграммы расположены кривые для слабых оснований, ниже линии нейтральности ( рН 7) - кривые слабых кислот. Кривые кислот и оснований с одинаковыми значениями рК зеркально симметричны относительно линии нейтральности. [32]
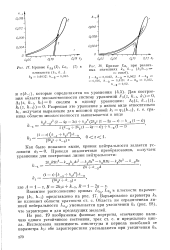 |
Кривые. Дз ( 1, La.| S. Крииые La3 при различных значениях А-3, к 3 ( &3 / А - з const. [33] |
Варьирование параметра Аз не изменяет области кратности ст. с. Область же ограниченная линией нейтральности Ь з, уменьшается при увеличении Аз ( рис. 18), что характерно и для предыдущих моделей. [34]
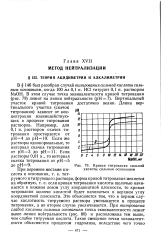 |
Кривая титрования сильной кислоты сильным основанием. [35] |
Это объясняется тем, что в первом случае кислотность титруемого раствора уменьшается в процессе титрования, а во втором случае увеличивается. При титровании слабой кислоты сильным основанием точка эквивалентности лежит выше линии нейтральности ( рис. 80) и расположена тем выше, чем слабее титруемая кислота. [36]
Графическая зависимость, вычисленная по уравнению (3.20) для разных рКкисл и рКосн, приведены на рис. 3.1. В верхней части диаграммы расположены кривые для слабых оснований, ниже линии нейтральности ( рН 7) - кривые слабых кислот. Кривые кислот и оснований с одинаковыми значениями рК зеркально симметричны относительно линии нейтральности. [37]
Аналогично описанному ведут определение и других кислот, как сильных, так и слабых, как неорганических, так и органических. Но следует помнить, что при титровании слабых кислот сильными щелочами точка эквивалентности лежит ниже линии нейтральности, и интервал скачка на кривой титрования сравнительно небольшой. Вследствие этого правильность выбора индикатора, в присутствии которого следует вести данное титрование приобретает очень большое значение ( см. стр. [38]
Аналогично описанному ведут определение в других кислот, как сильных, так и слабых, как неорганических, так и ор аниче-ских. Но следует помнить, что при титровании слабых кислот еиль-нымн щелочами точка эквивалентности лежит наже линии нейтральности, и интервал скачка на кривой титрования сравнительно небольшой. Вследствие этого правильность выбора индикатора, в присутствии которого следует вести данное титрование, приобретает очень большое значение ( см. стр. [39]
Целесообразно сохранить на этих линиях отдельные точки, отвечающие более сложным бифуркациям. Таким образом, имеет смысл изображать: а) линии кратности - совокупность всех точек ( ос, Р), для которых какое-нибудь нз положений равновесия имеет нулевое собственное число; б) линии нейтральности - совокупность всех точек ( ос, Р), для которых какое-нибудь положение равновесия имеет чисто мнимые собственные числа. [40]
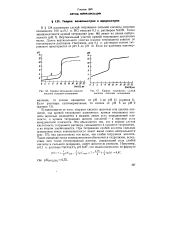 |
Кривая титрования сильной кислоты сильным основанием.| Кривая титрования слабой кислоты сильным основанием. [41] |
В зависимости от того, титруют кислоту щелочью или щелочь кислотой, ход кривой титрования изменяется: кривая титрования кислоты щелочью начинается в нижнем левом углу координатной плоскости, а кривая титрования щелочи кислотой - в верхнем углу координатной плоскости. Это объясняется тем, что в первом случае кислотность титруемого раствора уменьшается в процессе титрования, а во втором увел / ичивается. При титровании слабой кислоты сильным основанием точка эквивалентности лежит выше линии нейтральности ( рис. 67); она расположена тем выше, чем слабее титруемая кислота. Такое смещение точки эквивалентности объясняется гидролизом, вследствие чего точно оттитрованный раствор, содержащий соль слабой кислоты и сильного основания, имеет щелочную реакцию. [42]
Прямую, параллельную оси абсцисс и при рН 7 0 пересекающую ось ординат, называют линией нейтральности. Прямую, параллельную оси ординат и пересекающую ось абсцисс при V ( NaOH) 100 0 мл, называют линией эквивалентности: левее этой прямой находятся растворы, содержащие избыток кислоты, правее - избыток щелочи. Точку пересечения кривой титрования с линией эквивалентности называют точкой эквивалентности, а пересечение кривой титрования с линией нейтральности называют точкой нейтральности. Как видно, при титровании сильной кислоты сильным основанием точка эквивалентности и точка нейтральности совпадают. [43]
Для этого нужно степень оттитрованности увеличить в 100 раз. За зависимую переменную берут рН титруемого раствора. На сетке выделяют две важнейшие линии: линию нейтральности и линию эквивалентности. Далее вычисляют рН титруемого раствора в зависимости от степени его оттитрованности по соответствующим формулам, как это было выполнено в § 4 данной главы, и наносят их на сетку. [44]
Вместо степени оттитрованности берут также процент оттитрован ности. Для этого нужно степень оттитрованности увеличить в 100 раз. За зависимую переменную берут рН титруемого раствора. Чтобы вычертить кривую титрования необходимо подготовить сетку и нанести на нее соответствующие точки. На сетке выделяют две важнейшие линии: линию нейтральности и линию эквивалентности. [45]
Страницы: 1 2 3