Линия - равновесие
Cтраница 1
Линия равновесия часто значительно отклоняется от прямой. В этих случаях, во избежание ошибок, следует пользоваться более точным методом расчета, рассматриваемым ниже. [1]
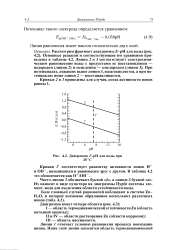 |
Диаграмма. Е - рН для воды при. [2] |
Линия равновесия имеет наклон относительно двух осей. [3]
Линия равновесия в этом случае имеет наклон. [4]
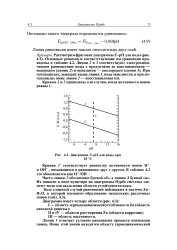 |
Диаграмма. 7 - рН для воды при. [5] |
Линия равновесия имеет наклон относительно двух осей. [6]
Линии равновесия ( ОС) и рабочая ( Л - В), используемые при графическом расчете массообменных процессов. [7]
Линия равновесия часто значительно отклоняется от прямой. В этих случаях, во избежание ошибок, следует пользоваться более точным методом расчета, рассматриваемым ниже. [8]
Линии равновесия построены для определенного давления, например для 760 мм рт. ст.. Способ построения изо-в треугольной диаграмме показан на фиг. [9]
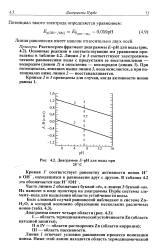 |
Диаграмма S - pH для воды при. [10] |
Линия равновесия имеет наклон относительно двух осей. [11]
Линии равновесия для реакций между минералами постоянного состава на диаграммах химических потенциалов будут прямыми, поскольку изменение химических потенциалов вполне подвижных ксмпонентов не влияет в данном случае на их количества, поглощаемые или выделяемые при реакции. Для реакций между минералами переменного состава линии равновесия могут быть кривыми, если изменение химических потенциалов вполне подвижных компонентов / и g изменяет их содержания в минералах, а следовательно, и количества, участвующие в реакции. [12]
Линии равновесия делят поле диаграммы на три области: магнетит, вюстит и железо. [13]
Линия равновесия фаз отделяет область, соответствующую составу однофазной или гомогенной системы, от области, где система распадается на два1 жидких слоя. [14]
Линия равновесия идеального процесса 1 проведена в соответствии с уравнением ( VI, 27) как диагональ квадрата; линия равновесия действительного процесса 2 построена по уравнению ( VI, 26) с использованием экспериментально найденных для этого случая значений А 1 02 и а - 0 00074; линии рабочих концентраций идеального и действительного процессов 3 и 4 проведены соответственно на основании уравнений ( VI29) и ( VI28) с применением одинаковых для всех ступеней значений di и различных для каждой ступени а, найденных из опыта. После нанесения на диаграмму всех перечисленных линий обычным способом построены ступени процесса в указанных выше пределах концентраций. [15]
Страницы: 1 2 3 4 5