Линия - характеристический рентгеновский спектр
Cтраница 1
Линии характеристического рентгеновского спектра немногочисленны. Для каждого элемента их число вполне определенное и индивидуальное. Достоинством анализа рентгеновского спектра является то, что относительная интенсивность большинства спектральных линий постоянна и основные параметры не зависят от химического состава соединений и смесей, в которые входит данный элемент. В то же время количество линий в спектре может зависеть от концентрации данного элемента. При предельно малых концентрациях элемента в спектре соединения появляются только две-три ярко выраженные линии. Для анализа соединений по спектрам необходимо знать не только длины волн основных линий, но и их относительную интенсивность. [1]
Какая из трех линий характеристического рентгеновского спектра - Кр, К, Ц - самая коротковолновая. [2]
В литературе имеются таблицы как линий характеристических рентгеновских спектров [15], так и критических энергий, соответствующих скачкам поглощения [16], с помощью которых всегда можно подобрать подходящие поглотители и исследовать природу электромагнитного излучения, сопровождающего процессы радиоактивных превращений. [3]
Анализ рентгеноспектральным методом осуществляется по линиям характеристического рентгеновского спектра. Анализ может быть проведен без разложения или разрушения образца, что является большим преимуществом метода. [4]
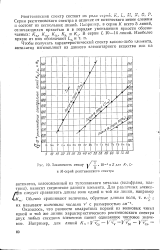 |
Зависимость между т /. 10 - 4 nZ для / С . [5] |
Оказалось, что разности квадратных корней из волновых чисел одной и той же линии характеристического рентгеновского спектра двух любых соседних элементов имеют одинаковое числовое значение. [6]
Смещение линий характеристического рентгеновского спектра при переходе от одних элементов к другим подчиняется закону Мозли: корень квадратный из частоты одной и той же линии линейно растет с порядковым номером элемента. Наиболее точно этот закон соблюдается для линий самой коротковолновой / ( - серии. [7]
 |
Рентгеновские спектры.| Зависимость частот / С-серии от порядкового номера. [8] |
Смещение линий характеристического рентгеновского спектра при переходе от одних элементов к другим подчиняется важному закону, открытому Мозли ( 1914): корень квадратный из частоты одной и той же линии линейно растет с порядковым номером элемента. Наиболее точно этот закон соблюдается для линий / С-серии. Все они лежат на прямых. Для линий L-серии соответствующие кривые несколько отступают от прямых, и эти отступления еще больше для линий высших серий. [9]
В 1913 г. Мозли разработал метод экспериментального определения величин зарядов ядер на основании измерения частот колебаний, отвечающих линиям характеристических рентгеновских спектров элементов, и ввел термин атомный помер, равноценный порядковому номеру. Он доказывает опытным путем, что заряды ядер атомов изменяются в соответствии с порядковыми номерами элементов в периодической системе. Устраняются кажущиеся неправильности расположения элементов в периодической системе, атомный номер иода оказывается выше атомного номера теллура, атомный номер никеля - больше атомного номера кобальта. [10]
Закон Мозли объясняет рассмотренная выше теория спектров Бора. Подобно тому как линии оптических видимых и ультрафиолетовых спектров элементов возникают в результате перескоков внешних электронов с более высоких к более низким уровням, линии характеристического рентгеновского спектра возникают в результате таких же перескоков внутренних, более близких к ядру электронов. Это отличие объясняет характерные различия между оптическими и рентгеновскими спектрами. Первые обнаруживают периодичность строения ( например сходство спектров всех щелочных или всех щелочноземельных металлов), объясняемую сходством строения внешней оболочки электронов. Такая периодичность отсутствует в внутренних слоях электронов: поэтому ее нет и в рентгеновских спектрах. Оптические спектры испытывают большие изменения при комбинации атомов в молекулы, так как при этом внешние электронные оболочки изменяют свое строение. Наоборот, при химических процессах не только ядро, но и внутренние электроны не затрагиваются, так как они экранированы от внешних воздействий слоем наружных электронов и, в соответствии с этим, на рентгеновские спектры мало влияют изменение агрегатного состояния элемента и его переход в то или иное соединение с другими элементами. Наконец, рентгеновские спектры значительно проще оптических потому, что для перескоков внутренних электронов предоставлено меньше возможностей, чем для внешних, ввиду того что большая часть внутренних уровней уже занята другими электронами. Теория Бора также легко объясняет, почему перескоки внутренних электронов дают значительно более коротковолновое излучение, чем перескоки внешних электронов. [11]
Быстрые электроны, проникая внутрь электронной оболочки атома, выбивают электроны, принадлежащие внутренним электронным слоям. Ближайший к ядру электронный слой ( К-слои) содержит два электрона. При переходе электрона с L-слоя на / ( - слой излучается наиболее интенсивная / С - линия характеристического рентгеновского спектра. Электроны L-слоя находятся в поле ядра с зарядом Ze, которое ослаблено одним электроном, оставшимся в / ( - слое. [12]
Страницы: 1