Технический ацетилен
Cтраница 2
Технический ацетилен содержит следующие примеси: фосфористый водород, сероводород, аммиак, кремнистый водород, воздух, водяные пары и др. Все они переходят из карбида кальция. Содержание примесей в ацетилене зависит от качества карбида кальция, способа разложения его и конструкции аппаратов, в которых его получают. [16]
Технический ацетилен, который используется для производства автогенных работ, имеет неприятный запах ( от примеси других соединений) и ядовит, подобно окиси углерода. [17]
Технический ацетилен содержит следующие примеси: фосфористый водород, сероводород, аммиак, кремнистый водород, воздух, водяные пары и др. Все они переходят из карбида кальция. Содержание примесей в ацетилене зависит от качества карбида кальция, способа разложения его и конструкции аппаратов, в которых его получают. [18]
Технический ацетилен для газопламенной обработки металла получают из карбида кальция непосредственно на строительной площадке с помощью ацетиленовых генераторов. Карбид кальция представляет собой продукт соединения кальция с углеродом при взаимодействии обожженной извести с коксом или антрацитом в электрических печах. [19]
Технический ацетилен при нормальном давлении и температуре представляет собой бесцветный горючий газ с резким запахом, обусловленным содержащимися в нем примесями сернистого водорода, фосфористого водорода, аммиака и др. Длительное вдыхание его вызывает тошноту, головокружение и даже отравление. Температура пламени при сгорании ацетилена в смеси с кислородом достигает 3200 С. При длительном соприкосновении ацетилена с медью и серебром образуются взрывоопасные соединения. При определенных соотношениях смесь ацетилена с воздухом или кислородом взрывоопасна. [20]
Технический ацетилен, применяемый для получения сажи, имеет следующий состав ( в объемн. [21]
Технический ацетилен освобождался от имеющихся в нем примесей ( главным образом, ацетона) при пропускании его через активированный уголь и двукратной сублимации. [22]
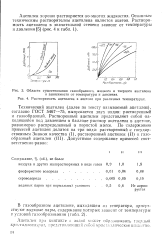 |
Области существования газообразного, жидкого и твердого ацетилена. [23] |
Технический ацетилен ( далее - по тексту называемый ацетилен), согласно ГОСТ 5467 - 75, выпускается двух видов: растворенный и газообразный. [24]
Технический ацетилен, применяемый для газопламенной обработки металлов, вследствие наличия в нем примесей имеет специфический неприятный запах. С и давлении 1 ата весит 1 09 кг; 1 ж3 воздуха при тех же условиях весит 1 33 кг. [25]
 |
Режим сушки грунтовок для умеренного климата. [26] |
Технический ацетилен ( ГОСТ 5457 - 75) и газообразный технический кислород ( ГОСТ 5583 - 78) применяют для газовой сварки. Аргон, ацетилен и кислород и другие газы поставляют в стальных баллонах ( ГОСТ 949 - 73), имеющих соответствующую окраску. [27]
Технический ацетилен, наряду с указанными примесями, обычно содержит некоторое количество воздуха. Получить ацетилен, совершенно свободный от воздуха, не удается даже при применении генераторов наиболее совершенной конструкции. Присутствие же в ацетилене больших количеств воздуха создает опасность образования взрывчатых ацетилено-воздушных смесей. [28]
Технический ацетилен при нормальном давлении и температуре представляет собой бесцветный горючий газ с резким запахом, обусловленным содержащимися в нем примесями сернистого водорода, фосфористого водорода, аммиака и др. Длительное вдыхание его вызывает тошноту, головокружение и даже отравление. Температура пламени при сгорании ацетилена в смеси с кислородом достигает 3200 С. При длительном соприкосновении ацетилена с медью и серебром образуются взрывоопасные соединения. При определенных соотношениях смесь ацетилена с воздухом или кислородом взрывоопасна. [29]
Технический ацетилен CzHz при сжигании дает температуру пламени 3150 С. Для технических целей ацетилен поставляют в готовом виде в баллонах или получают на месте строительства путем соединения карбида кальция с водой. [30]
Страницы: 1 2 3 4