Жидкий ацетилен
Cтраница 3
Заслуживают внимания результаты, полученные для ацетилена, так как для него сдвиг при переходе от жидкости к газу больше, чем для аммиака. Хотя обычно предполагают, что в жидком ацетилене водородных связей нет, имеющиеся данные по инфракрасным спектрам указывают на то, что я-связь ацетиленовых и в меньшей степени этиленовых молекул может способствовать образованию водородных связей в таких системах. Наиболее детально изучены водородные связи между атомами О; расстояния О - О колеблются между 2 40 и примерно 3 00 А, а энергии составляют около 5 ккал / моль. Предполагается, что во всех таких связях, за исключением самых коротких, протон находится в потенциальном поле с двумя минимумами. Это означает, что в каждый момент он связан в основном либо с одним, либо с другим атомом О. [31]
При больших разбавлениях фактор мощности еще более снижается, например при добавлении 20 % разбавителя он делается меньше единицы. При использовании же детонатора кордтекс, чтобы сделать жидкий ацетилен невзрывчатым веществом ( фактор мощности меньше 10), необходимо добавить 40 % разбавителя. [32]
Использование в качестве среды для проведения процесса этинилирования диэтилового эфира удобно в лабораторных условиях, но крайне нежелательно в производственных условиях из-за высокой летучести и легкой воспламеняемости. Хотя выбору растворителя посвящено много работ ( предложено проводить реакцию даже в жидком ацетилене [18]), на практике предпочтение обычно отдают толуолу, поскольку в этом случае достаточно просто решается проблема удаления воды из щелочи путем азеотроп-ной отгонки. Большими потенциальными возможностями обладают в этом отношении простые эфиры гликолеи и ацетали, позволяющие проводить плавление щелочи под слоем этих веществ при температуре всего 120 - 140 С. [33]
Данные о распространении распада ацетилена из газовой фазы в жидкую приведены в табл. 12.2. Во всех случаях, за исключением одного, детонация, возникающая в газе, переходила затем в жидкость. При добавлении 12 % ацетона или 16 % двуокиси углерода скорость детонации в жидком ацетилене была примерно одинаковой. При добавлении 25 % ацетона или 30 % двуокиси углерода скорость уменьшалась, но все же была достаточно большой. [34]
Данные о распространении распада ацетилена из газовой фазы в жидкую приведены в табл. 3.23. Во всех случаях, за исключением одного, детонация, возникающая в газе, переходила затем в жидкость. При добавлении 12 % ацетона или 16 % двуокиси углерода скорость детонации в жидком ацетилене была примерно одинаковой. При добавлении 25 % ацетона или 30 % двуокиси углерода скорость уменьшалась, но все же была еще достаточно большой. [35]
Такое увеличение объема сравнимо с увеличением объема при смешении ацетона с жидким ацетиленом. Например, при атмосферном давлении и - 80 С в 1 г ацетона растворяется 1 3 г жидкого ацетилена. [36]
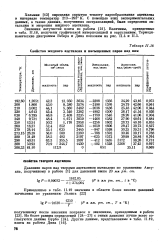 |
Свойства жидкого ацетилена и насыщенных паров над ним. [37] |
С помощью этих экспериментальных данных, а также данных, полученных экстраполяцией, были определены энтальпия и энтропия жидкого ацетилена. [38]
При адсорбции ацетилена на поверхности окиси алюминия Иейтс и Луккези ( 1961) нашли полосу поглощения валентного колебания углерод - углерод, обычно запрещенную в инфракрасном спектре. Частоты этих полос могут быть сопоставлены с полосами поглощения при 1974 и 1961 см 1, наблюдавшимися в спектре комбинационного рассеяния для газообразного и жидкого ацетилена соответственно. [39]
Следовательно, при охлаждении газообразный ацетилен превращается в твердое вещество; однако при небольшом давлении твердый ацетилен может быть превращен в жидкость. Жидкий ацетилен весьма чувствителен к механическим ударам, а следовательно, является очень взрывоопасным. [40]
При реакции ацетилена с кипящей серой, как было найдено [38], образуется H2S, CS2 и следы тиофена, а при реакции с HCN в горячей трубке [39] - цианистый аммоний и пиррол. Сообщалось также [40] об образовании стирола из бензола и ацетилена в присутствии хлористого аммония, однако этот результат не был подтвержден впоследствии. Жидкий ацетилен был получен Кайетэ [41], а Энсделл [42] изучил его физические свойства. [41]
Чистый ацетилен представляет собою бесцветный газ с приятным эфирным запахом. При низких температурах он затвердевает в белую Кристаллическую массу с темп. Жидкий ацетилен по данным Mclntosh a и Maass a12 кипит при - 88 5, но другие исследователи дают следующие температуры - 82 4 13 и - 84 и. Он имеет следующие критические константы: критическая температура 37 05, критическое давление 68 0 ат, критический объем 83 смя. [42]
Баллоны заполняют пористой массой, адсорбирующей раствор ацетилена; при этом ацетон растворяет около 300 объемов ацетилена. Разложение жидкого ацетилена со взрывом происходит под влиянием тепла, ударов, трения, сжатия, под действием запала. В смеси с кислородом ацетилен взрывает при атмосферном давлении. В смеси с хлором ацетилен взрывает уже под действием света. [43]
Осушка холодом может быть применена для ацетилена низкого и среднего давления. Однако при производстве растворенного ацетилена осушка холодом неприемлема, так как при высоком давлении ацетилен легко сжижается при понижении температуры. Образование жидкого ацетилена в аппаратуре под высоким давлением весьма опасно. Кроме того, при этих условиях может накапливаться кристаллогидрат ацетилена. [44]
С энергия увеличивается примерно в 30 раз. Энергия зажигания жидкого ацетилена при давлениях 1 4 - 12 2 ат изменяется в пределах 11 - 0 13 дж, а газообразного при аналогичных давлениях и Т 20 С в пределах 8 - 0 002 дж. Таким образом, энергия зажигания жидкого ацетилена близка к энергии зажигания газообразного ацетилена при низких начальных давлениях ( 1 4 ат), но значительно больше при высоких. Это, вероятно, объясняется тем, что при инициировании ацетилена в жидкой фазе некоторая ( примерно постоянная) часть энергии зажигания тратится на испарение ацетилена. При наличии газовых включений, например при кипении жидкости, следует ожидать дальнейшего уменьшения величины энергии зажигания с повышением давления. Вследствие этого процесс газификации ацетилена представляет наибольшую опасность. [45]
Страницы: 1 2 3 4