Линтон
Cтраница 2
Между прочим, аномальная проводимость ионов ОН - также основывается на механизме перехода протонов как на одном из видов протонно-дырочной проводимости, причем, согласно Конвею, Бокрису и Линтону [7], скорость процесса определяется переориентацией молекул воды после происшедшего перехода. [16]
Экспериментальные данные по турбулентной диффузии при больших числах Прандтля ( Шмидта) берутся из исследования в диффузионной области двоякого рода процессов: электродных реакций и процессов растворения. Линтон и Шервуд [16] изучали растворение в воде внутренних поверхностей малых полых цилиндриков из 3-наф-тола, бензойной и коричной кислот. [17]
Экспериментальные данные по турбулентной диффузии при больших числах Прандтля ( Шмидта) берутся из исследования в диффузионной области двоякого рода процессов: электродных реакций и процессов растворения. Линтон и Шервуд [16] изучали растворение в воде внутренних поверхностей малых полых цилиндриков из ( - наф-тола, бензойной и коричной кислот. [18]
Линтон, один из авторов концепции социального статуса и социальной роли, подчеркивал, что для науки понятие статус неотделимо от понятия роль - это по сути две стороны одной медали. Соответствующая теория, описывающая социальное поведение личности, называется статусно-ролевой теорией личности. Вместе с тем имеется ощутимое, хотя и условное, различие этих понятий. Если статус есть фиксация определенной социальной позиции ( его содержательного, диспозиционного, номинационного аспектов), т.е. статус статичен, то роль - это динамическая характеристика, определяющая, как должен вести себя человек, обладающий тем или иным статусом. [19]
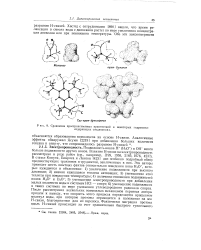 |
Сравнение пространственных препятствий в некоторых гидроксил. [20] |
В статье Конуэя, Бокриса и Линтон [423 ] дан особенно подробный обзор предшествующих трактовок и трудностей, заключенных в них. Эти авторы приводят шесть опытных фактов относительно поведения иона Н3О % которые нуждаются в объяснении: 1) увеличение подвижности при высоком давлении; 2) низкая кажущаяся теплота активации; 3) уменьшение этой теплоты при повышении температуры; 4) величина отношения подвижностей ионов НзО и D3O; 5) уменьшение электропроводности при добавлении малых количеств воды к системам НС1 - спирт; 6) уменьшение подвижности в таких системах по мере удлинения углеводородного радикала спирта. После рассмотрения нескольких возможных механизмов переноса авторы пришли к выводу, что скорость этого процесса определяется вращением молекул воды, при котором протоны переводятся в положение на оси Н - связи, благоприятное для их переноса. [21]
Однако механизмы прототропной проводимости ионов водорода и гидроксила значительно различаются. По теории Конуэя, Бокриса и Линтона [49] скорость переноса протона в водных растворах определяется вращением молекул воды как диполей во внутренней гидратной оболочке ионов, обеспечивающим возможность следующего переноса протона ( собственно перенос протона вдоль водородной связи, соединяющей соседние молекулы воды, - процесс быстрый), так как немедленно вслед за переносом протона ориентация соседних молекул воды неблагоприятна для переноса. Молекулы воды достигают положения, при котором возможен перенос протона, только после вращения. Однако возникшие в результате вращения молекул растворителя взаимодействия вблизи ионов оксония и гидроксила различны. [22]
При этом, конечно, предполагается, что время жизни сравнимо с обратной величиной частоты колебаний. Кинетические расчеты Конуэя, Бокриса и Линтона [51], теоретически предсказавших значительное время жизни иона Н3О, привели Фалка и Жигера [34] к необходимости возобновить усилия по получению ИК-спектра этих частиц в концентрированных жидких водных растворах хлористого водорода и других кислот. [23]
В первой из этих работ авторы без каких-либо пояснений вводят в ( 25 20) определенный числовой коэффициент. В широко цитируемых в химической литературе и литературе по теплопередаче работах Линтона и Шервуда [6], Мильтона и Кольбэрпа [7] и Лина и др. [8] указывается, что можно получить согласие теоретических формул с опытом, если принять ( 25 20) как некоторую эмпирическую формулу. [24]
Рассмотренная выше теория [51] была первой попыткой априорного расчета относительных скоростей отдельных стадий подвижности протона без использования эмпирических приближений. Эйген и де Майер [93], которые фактически поддержали механизм, предложенный Конуэем, Бокрисом и Линтоном, сделали ряд замечаний относительно этих расчетов. Они рассмотрели вопрос о квантовом распределении и показали, что использование квантового описания энергетических состояний протона, приближающегося к барьеру, не влияет существенно на величину расчетной подвижности - туннельный переход происходит гораздо быстрее, чем структурная реориентация - и не может достаточно обоснованно объяснить изотопный эффект. [25]
Предшествующие исследователи, основываясь на химических свойствах и аналогии, предположили, что продуктом реакции SiH3I с AgCN является изоцианид. Линтон и Никсон, предполагая, что в этой реакции образуется нормальный цианид, синтезировали образцы, обогащенные 13С и SN. [26]
Установленные Линтоном различия позволили представить общество в виде четко ограниченных переменных: природы и вида взаимодействий между позициями и видами экспектаций, связанных с этими позициями. [27]
Яркий пример - кровавое побоище в средней школе Линтона ( штат Колорадо), когда было убито 25 учеников и 20 ранено. [28]
Как уже говорилось выше, предложенный Хюккелем механизм вращения иона Н3О неприменим, помимо других причин, еще и потому, что из таких представлений следует выводе необходимости последовательного вращения молекул воды. Поскольку очевидно, что эта модель является неудовлетворительной, Конуэй, Бокрис и Линтон [51] провели детальный анализ процесса вращения молекул воды в качестве альтернативного механизма, определяющего скорость переноса протона. [29]
В 1932 г. Линтон и Маас [13] определили дипольный момент перекиси водорода методом разбавления, использовав в качестве растворителей диоксан и этиловый эфир. Найденные значения, по их мнению, подтверждают правильность плоскостной тригональной модели. Линтона и Мааса приведены некоторые возражения, однако эти возражения не могут поколебать в значительной мере полученные значения. Эти значения дипольного момента экспериментально подтвердили Масси и Бьянко [20], показавшие, что их наблюдения эффекта Штарка в микроволновом спектре перекиси водорода согласуются с дипольным моментом 2 26 - 10 - 18 CGSE. Эти значения дипольного момента, безусловно, исключают возможность линейной цепной и транс-плоскостной цепной моделей. [30]
Страницы: 1 2 3