Фтористый литий
Cтраница 3
 |
Кристаллы хлористого натрия. [31] |
Электропроводность расплавленных фтористого лития и хлористого натрия можно легко измерить. Она ниже, чем у металлов, на несколько порядков. Расплавленный хлористый натрий при 750 С имеет электропроводность, составляющую лишь КГ9 электропроводности металлической меди при комнатной температуре. Маловероятно, что электрический заряд в расплавленном NaCl перемещается по тому же механизму, что и в металлической меди. [32]
О растворимости фтористого лития в водных растворах фтористого водорода определенных данных нет; предполагают, что растворимость фтористого лития в плавиковой кислоте немного больше, чем в воде. [33]
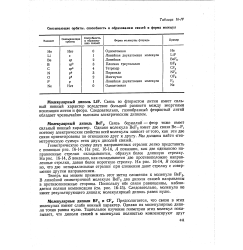 |
IV Связывающие орбиты, способность к образованию связей и форма молекул. [34] |
Связь во фтористом литии имеет сильный ионный характер вследствие большой разности между энергиями ионизации лития и фтора. Следовательно, газообразный фтористый литий обладает чрезвычайно высоким электрическим диполем. [35]
Хлористый натрий и фтористый литий повышают электропроводность электролита. Фтористый кальций и в несколько меньшей степени фтористый магний повышают его плотность и вязкость, фтористый литий и хлористый натрий понижают плотность и вязкость. [36]
Ионные вещества, например фтористый литий и хлористый натрий, образуют кристаллы правильной формы с четкими гранями. Чистые кристаллы таких твердых веществ обычно прозрачны и бесцветны, но они могут быть окрашены очень небольшими добавками примесей. Такое же действие оказывают и дефекты, имеющиеся в кристаллической решетке. Большинство ионных кристаллов имеет высокие температуры плавления. [37]
При облучении нейтронами фтористого лития получающийся тритий отделяют нагреванием мишени в вакууме. Водород превращают в воду, пропуская его над окисью меди. [38]
Следовательно, молекулы фтористого лития более устойчивы, когда они построены так, что каждый атом лития расположен одновременно около нескольких атомов фтора: так же как и в металлах, атом со свободными орбитами более устойчив, если он окружен несколькими соседними атомами. Тогда электроны, удерживаемые соседними атомами, могут находиться одновременно около двух или более ядер. Но в данном случае имеется существенное отличие от металлов - в твердом фтористом литии половина атомов обладает высокой энергией ионизации. Атомы фтора прочно удерживают свои электроны. Поэтому в ионных кристаллах характерная для металлов подвижность электронов отсутствует. Это означает, что у ионных кристаллов нельзя ожидать проявления металлических свойств. Посмотрим, какие же свойства имеют эти вещества. [39]
Результаты исследования вискерсов фтористого лития, сходного по своему строению и механическим свойствам с периклазом, представляют большой интерес для познания особенностей вискерсов раскола окиси магния. [40]
Состав продуктов испарения фтористого лития, вычисленный в предположении, что энергия диссоциации димера равна 61 ккал / моль и содержание тримера при 900 - 1300 К составляет 15 % [62, 63], а при. В последнем столбце табл. 268 даны значения теплоты сублимации мономерных молекул LiF, вычисленные с учетом сложного состава паров. [41]
Значения теплоты сублимации фтористого лития, вычисленные по данным, полученным в работах [3344, 3687, 3562, 4170, 62], находятся в удовлетворительном согласии и приводят к среднему значению АЯ50 65 ккал / моль. [42]
 |
Оптическая схема спектрофотометра ИКС-14А. [43] |
Линзы изготовляются из фтористого лития и бромистого калия. [44]
Первоначально было изучено влияние фтористого лития на свойства электролита. Предварительные опыты показали, что добавление нескольких процентов фтористого лития к электролиту понижает температуру плавления, без каких, либо других изменений свойств электролита. [45]
Страницы: 1 2 3 4 5