Логарифм - константа - равновесие - реакция
Cтраница 1
Логарифм константы равновесия реакции при рН 2 0 равен 4 8, изменение свободной энергии образования соединения при 25 С составляет - 6 6 ккал / моль. [1]
Кривые логарифмов констант равновесия реакций образования сложных окислов пересекают нулевую линию. Точки пересечения отвечают химическому равновесию и соответственно термодинамическому равновесию систем. [2]
Показано, что логарифмы констант равновесия реакций дегидрирования в зависимости от обратной величины температуры образуют прямые линии, расходящиеся при низких температурах. Эти линии пересекают нулевое значение логарифма константы в пределах температур 1670 - 930 К. [3]
В рассматриваемом интервале температур логарифмы констант равновесия реакций гидрогенолиза почти всех сернистых соединений представляют собой большие положительные величины. Таким образом, в присутствии стехиометрических количеств водорода реакция почти в любом случае может протекать до практически полного завершения. При гидрогенолизе тиофена с образованием н-бутана и сероводорода глубина реакции ограничивается термодинамическим равновесием. [4]
В этом же интервале температур логарифм константы равновесия реакции прямого восстановления меняет свой знак с отрицательного на положительный, и термодинамическая невозможность реакции сменяется самопроизвольным процессом восстановления при достаточно высоких температурах. [5]
Основность молекулы В определяется либо логарифмом константы равновесия реакции ( 2), протекающей в водной фазе ( рКа либо энтальпией реакции ( 1), протекающей в газовой фазе. [6]
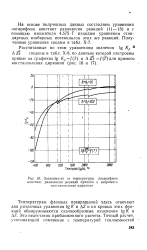 |
Зависимость от температуры логарифмов. [7] |
На основе полученных данных составляем уравнения логарифмов констант равновесия реакций ( 1) - ( 5) и с помощью множителя 4 575 - Т находим уравнения стандартных изобарных потенциалов этих же реакций. [8]
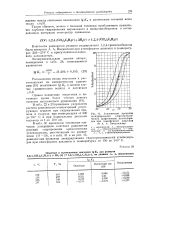 |
Равновесные проценты дегидрирования гидроароматических ( нафтеновых углеводородов при атмосферном давлении по А. А. Введенскому. [9] |
В табл. 30 приведены численные значения логарифмов констант равновесия реакций гидрирования ароматических углеводородов, рассчитанные по уравнениям ( 11 - 19), а в табл. 31 и на рис. 13, равновесные проценты дегидрирования гидроароматических углеводородов при атмосферном давлении и температурах от 150 до 500 С. [10]
Ван Эйк и ван Форгуизен [4] приводят логарифмы констант равновесия реакций изомеризации 2-метилпентана в другие изомеры гексана. [11]
Расстояние между обеими пологими ветвями определяется чис-ленным значением логарифма константы равновесия реакции титрования. [12]
Расстояние между обеими пологими ветвями определяется численным значением логарифма константы равновесия реакции титрования. [13]
Из рис. 6 и 7 следует, что как логарифм константы равновесия реакции раскисления, так и ее изобарный потенциал связаны с концентрацией расплава гиперболической зависимостью. При значительном разбавлении расплава численные значения логарифмов констант равновесия реакции резко снижаются, а изобарных потенциалов - возрастают. [14]
В 1936 г. Д. М. Рудковский [2] вычислил по приближенному уравнению Нериста логарифмы констант равновесия реакций образования этиламина, пропиламина, изоамиламина, вторичного бутиламина и нормального бутиламина из аммиака и олефинов для интервала 25 - 300 С. Автор пришел к выводу, что прямой синтез этиламина из аммиака и этилена может быть осуществлен в указанном интервале температур с хорошими выходами, достигающими - 50 %, под давлением 100 атм и выше. Синтез пропиламина и более высокомолекулярных аминов также может быть осуществлен с выходами - 100 - 50 % даже при атмосферном давлении. [15]
Страницы: 1 2