Логарифм - растворимость
Cтраница 1
Логарифм растворимости AgC ] и CsCl по нашим данным, полученным в работе совместно с В. С. Черным [29] и по данным Вальдена для K. J и Et4NJ [19] в растворителях с не очень низкими ДП линейно зависит от I / O. При этом данные для растворимости в спиртах образуют одну прямую, а в кетонах - другую. [1]
 |
Средний коэффициент активности ацетата серебра в насыщенном растворе.| Растворимость соли Ва ( Ю3 2 Н2О в смесях диок-сан-вода. [2] |
Откладывая логарифм растворимости по оси ординат, а логарифм диэлектрической проницаемости растворителя по оси абсцисс, получают кривую, подобную изображенной на рис. 12 - 6 для Ва ( Ю3) 2 - Н2О в смесях диоксана с водой. Экспериментальные величины можно сравнить с вычисленными по уравнению Борна и по эмпирическому приближенному расчету, основанному на постоянстве коэффициента активности. В данном случае эмпирический расчет дает вполне удовлетворительный результат. [3]
 |
Растворимость соли Ba ( IOs2 - H2O в смесях диоксан - - вода. [4] |
Откладывая логарифм растворимости по оси ординат, а логарифм диэлектрической проницаемости растворителя по оси абсцисс, получают кривую, подобную изображенной на рис. 10 - 6 для Ва ( Ю) 2 - Н2О в смесях диоксана с водой. Экспериментальные величины можно сравнить с вычисленными по уравнению Борна и по эмпирическому приближенному расчету, основанному на постоянстве коэффициента активности. В данном случае эмпирический расчет дает вполне хороший результат. [5]
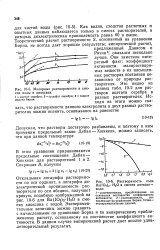 |
Растворимость соли Ba ( IOa2 H2O в смесях диоксан - вода. [6] |
Откладывая логарифм растворимости по оси ординат, а логарифм диэлектрической проницаемости растворителя по оси абсцисс, получают кривую, подобную изображенной на рис. 10 - 6 для Ва ( Юз) 2 - Н20 в смесях диоксана с водой. [7]
 |
Растворимость соли Ва ( Ю3 2 - Н2О в смесях диоксан - - вода. [8] |
Откладывая логарифм растворимости по оси ординат, а логарифм диэлектрической проницаемости растворителя по оси абсцисс, получают кривую, подобную изображенной на рис. 10 - 6 для Ва ( Юь) 2 - Н2О в смесях диоксана с водой. Экспериментальные величины можно сравнить с вычисленными по уравнению Борна и по эмпирическому приближенному расчету, основанному на постоянстве коэффициента активности. В данном случае эмпирический расчет дает вполне хороший результат. [9]
Откладывая логарифм растворимости по оси ординат, а логарифм диэлектрической проницаемости растворителя по оси абсцисс, получают кривую, подобную изображенной на рис. 10 - 6 для Ba ( IOi. Экспериментальные величины можно сравнить с вычисленными по уравнению Борна и по эмпирическому приближенному расчету, основанному на постоянстве коэффициента активности. В данном случае эмпирический расчет дает вполне хороший результат. [10]
Зависимость логарифма растворимости газа InN от 1 / Т описывается уравнением прямой. Это позволяет графически устанавливать зависимость растворимости газа в воде от температуры. [11]
Построена зависимость логарифма растворимости Кг в жидком In от обратной температуры [1], согласно которой растворимость изменяется от 1 56 - 10 - 8 до 5 6 - Ю-7 см3 на 1 смя соответственно при 1000 и 1300 С [ 10 9 - 1Q - 10 и 3 9 - 10 - 8 % ( ат. [12]
Линейная зависимость логарифма растворимости молекул кислот от 1 / е свидетельствует о том, что в ряду растворителей одной природы величина энергии взаимодействия неполярного радикала аниона с растворителем, вероятно, также является линейной функцией от величины, обратной величине диэлектрической проницаемости. Этим объясняется то обстоятельство, что с увеличением радикала аниона соли линейная зависимость lg у0 от 1 / е сохраняется в ряду растворителей одной природы. Величина радикала аниона сказывается только на изменении величины угла наклона и его знака. [13]
 |
Диаграмма. ионные радиусы - растворимости солей типа МеХ ( числа на кривых - значения vRT lg а, ккал / моль. [14] |
Линейная зависимость логарифма растворимости молекул кислот от 1 / е свидетельствует о том, что в ряду растворителей одной природы величина энергии взаимодействия неполярного радикала аниона с растворителем, вероятно, также является линейной функцией от величины, обратной величине диэлектрической проницаемости. Этим объясняется то обстоятельство, что с увеличением радикала аниона соли линейная зависимость lgY0 от 1 / е сохраняется в ряду растворителей одной природы. Величина радикала аниона сказывается только на изменении величины угла наклона и его знака. [15]
Страницы: 1 2 3 4