Лучи - кристаллизация
Cтраница 1
 |
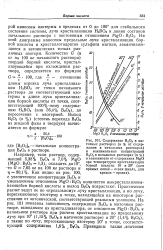
Центральная проекция изотермы простой четверной системы в случае, когда одна из солей ( В образует кристаллогидрат. [1] |
Лучи кристаллизации в поле безводной соли В являются продолжением лучей кристаллизации в поле кристаллогидрата, так как исходят из одной вершины ( полюса) В. [2]
Лучи кристаллизации в поле глазерита исходят из точки его состава s, расположенной за пределами поля ( ср. [3]
Лучи кристаллизации нитрата исходят из точки М его состава до пересечения с границей поля ВР. [4]
Лучи кристаллизации Ca ( NO3) 2 - 4H2O на горизонтальной проекции выходят из фигуративной точки М нитрата кальция и направляются до пересечения с границей поля ВР. На линии ВР лежат точки, которые характеризуют составы растворов, насыщенных одновременно двух - и четырехводным нитратом кальция. Это точки соответствуют максимально возможному выходу каждого исходного комплекса, теоретически лежащего на диагонали 6HNO3 - Ca3 ( PO4) 2 - Однако в природных фосфатах ( в частности, в апатите) мольное отношение ЗСаа: 2РО1 - несколько выше теоретического, поэтому точки, характеризующие составы исходных комплексов ( вытяжек, полученных разложением апатита азотной кислотой), лежат не на диагонали, а в области с более высоким содержанием кальция. [5]
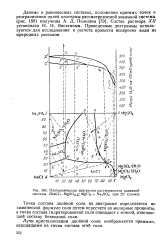 |
Изотермическая диаграмма растворимости взаимной системы 2NaCl MgSO4. MgCl2 Na2SO4 при 25 ( схема. [6] |
Лучи кристаллизации двойной соли изображаются прямыми, исходящими из точки состава этой соли. [7]
Эти предельные лучи кристаллизации ME и DE ограничивают два поля кристаллизации указанных солей. Характерная особенность этой системы, а также системы MgO - Р2О5 - Н2О - инконгруэнтность, когда составы жидких и твердых фаз не совпадают. [8]
Действительно, лучи кристаллизации исходят из бесконечности, так как по общему правилу они должны исходить из точки состава выпадающих твердых фаз. Только фигуративные точки состава гидратов откладывают на координатных осях, используя величины содержания в них воды. Конечное значение имеют только длины лучей испарения раствора и кристаллизации гидратов. Поэтому здесь неприменимо правило рычага для графического расчета процесса кристаллизации. Графический расчет возможен для количества испаряемой воды и при кристаллизации ( растворении) гидратов. [9]
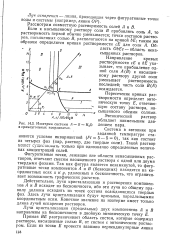 |
Изотерма системы А - В - Н2О в прямоугольных координатах. [10] |
Действительно, лучи кристаллизации и растворения компонентов Л и В исходят из бесконечности, ибо эти лучи по общему правилу должны исходить из точек состава осаждающихся твердых фаз. [11]
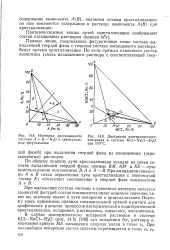 |
Изотерма растворимости системы А - В - Н2О в прямоугольном треугольнике.| Диаграмма изотермического испарения в системе КС1 - NaCl - Н2О при 110 С. [12] |
По общему правилу лучи кристаллизации исходят из точки состава выпадающей твердой фазы: прямые ВМ, AM и КБ - лучи кристаллизации компонентов В, А и А - В. При выпадании совместно А и В точка пересечения луча кристаллизации с гипотенузой ( точка К) обозначает соотношение в твердой фазе компонентов А и В. [13]
На этой диаграмме нанесены предельные лучи кристаллизации борной кислоты и кристаллогидратов сульфата магния, заканчивающиеся в эвтонических точках различных изотерм. [15]
Страницы: 1 2 3 4