Магний-ион
Cтраница 1
Магний-ион осаждают, каТс обычно, в виде MgNH4PO4 ( стр. [1]
Магний-ион соответствующего аниона в водном растворе определяют титрованием раствором трилона Б в присутствии индикатора кислотного хром черного до появления синей окраски. [2]
 |
Номограмма для расчетов при подкислении воды. [3] |
Вследствие этого концентрация магний-иона не может измениться при подогреве воды и в любых условиях работы теплосети будет равна концентрации его в исходной воде. [4]
Исследована зависимость концентрации магний-иона в жидкой фазе от содержания тригидрокарбоната магния, времени, температуры, добавки гидроокиси и основного карбоната магния. [5]
Показана связь изменения концентрации магний-иона в жидкой фазе и особенностей кристаллизационного структурообразования карбонатмагниевого материала. [6]
Воды из верховых торфов содержат магний-ион до 5 мг / л, но воды из субстрата тех же верховых фитоценозов отличаются уже значительно повышенным его содержанием. Так, воды, отжатые из очеса, составленного верховыми сфагновыми мхами, содержат около 7 мг / л магний-иона. В целом же показатель магния, как и кальция, вполне устойчив и может служить основой для определения типа минерального питания: до 5 мг / л - верховая стадия, от 3 мг / л и выше - низинная. [7]
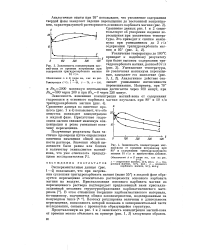
Представленную на рис. 1 и 2 зависимость концентрации магний-иона от времени м: ожно объяснить на примере ( рис. 1, 2) следующим образом. [9]
Проверьте подсчетом, можно ли получить положительную реакцию на магний-ион в насыщенном растворе гидроокиси магния в 2 М растворе хлорида аммония. [10]
 |
Зависимость концентрации магний-иона от времени нагревания при 80.| Зависимость концентрации магний-иона от времени нагревания при 95. [11] |
Из колбы периодически отбирались пробы жидкой фазы, которые анализировались на концентрацию магний-иона трилономет-рическим методом. [12]
Поскольку ионы металла Ме2 образуют с ЭДТА более устойчивое комплексное соединение, чем ионы Mg2, то высвободившийся в Эквивалентном количестве магний-ион оттитровывают раствором ЭДТА, как обычно с соответствующим индикатором. Расход раствора ЭДТА, затраченного на титрование иона Mg2, соответствует количеству определяемого иона, как и при прямом титровании. [13]
В результате интенсивного разложения количество тригидрокарбоната уменьшается, основного карбоната увеличивается, поэтому к 40 - 100 минутам скорости процессов перехода вещества в раствор и из раствора сближаются, а концентрация магний-иона достигает максимума. [14]
Ион натрия обладает наименьшим зарядом и наибольшим размером. Магний-ион имеет меньшие размеры, и заряд его больше. Следовательно, в Mg ( OH) 2 ионы кислорода притягиваются ионом магния сильнее, чем ионом натрия в NaOH; поэтому способность отщеплять ионы ОН ослаблена: Mg ( OH) 2-более слабое основание, чем NaOH. Пунктирные линии показывают, в каком месте происходит разрыв гидроокиси при электролитической диссоциации. Ион алюминия имеет еще больший заряд при меньшем размере иона. [15]
Страницы: 1 2