Концентрационно-логарифмическая диаграмма
Cтраница 1
Концентрационно-логарифмические диаграммы удобны для выяснения влияния одноименного иона при постоянной ионной силе раствора. Однако введение в раствор значительных количеств электролита, содержащего одноименный ион, вызывает заметные изменения ионной силы. Расчеты в подобных случаях следует вести по термодинамической константе растворимости. [2]
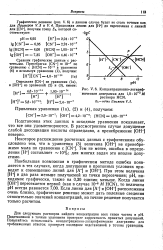 |
Концентрационно-логарифмическая диаграмма для 1 0 10 - 3АГ. [3] |
Попытайтесь использовать концентрационно-логарифмические диаграммы для приближенных ответов; проверьте последние подстэновкой в точные уравнения. [4]
Из изложенного следует, что концентрационно-логарифмическую диаграмму можно построить без проведения каких-либо расчетов. Для этого в системе координат pS - рН проводят горизонтальную прямую с ординатой - lg с. Она называется точкой системы. Через эту точку соединяют прямую с наклоном 1 с отрезком горизонтальной прямой левее точки системы, а также прямую с наклоном - 1 с отрезком горизонтальной прямой правее точки системы. На диаграмме обычно еще проводят прямую через точку с координатами ( 0; 0) и имеющую наклон 1; она показывает рН раствора, а также прямую, проходящую через точку с координатами ( 14; 0) и имеющую наклон - 1; она показывает рОН раствора. [5]
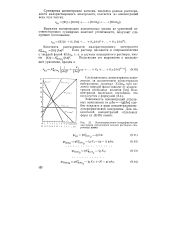 |
Концентрационно-логарифмическая диаграмма насыщенных водных растворов гид-роксида цинка. [6] |
An ] удобно показать в виде концентрационно-логарифмической диаграммы. [7]
 |
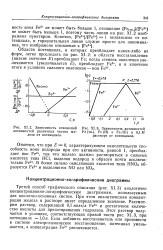
Распределитель - Рис Построение кривой титрования по конная диаграмма H2S03 центрационно-логарифмической диаграмме. [8] |
Еще проще построить кривую титрования по концентрационно-логарифмической диаграмме ( для построения такой диаграммы не нужно рассчитывать рН, см. разд. [9]
 |
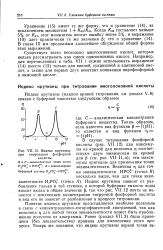
Зависимость отношений [ IMAGE ] 3. Зависимость активностей активностей различных частиц же - Ре ( тв., Fe ( II и Fe ( III в 0 1 М леза от потенциала. растворе от потенциала. [10] |
Третий способ графического описания ( рис. XI.3) аналогичен концентрационно-логарифмическим диаграммам, используемым для кислотно-основных систем. При этом аналитическая концентрация железа в растворе имеет определенное значение. Рассмотрим раствор, содержащий 0 1 моль ] л Fe3 и достаточное количество кислоты для предотвращения-гидролиза. Этот раствор получается в условиях, соответствующих правой части рис. XI. Если добавить восстановитель или произвести в системе электрохимическое восстановление, потенциал уменьшается, а концентрация Fe2 увеличивается. [11]
Сформулируем теперь общее правило: если точка пересечения на концентрационно-логарифмической диаграмме соответствует эквивалентной точке титрования, то расстояние от этой точки до горизонтальной основной линии для IgCo, уменьшенное на единицу в логарифмической шкале дает логарифм индекса крутизны в эквивалентной точке. [12]
 |
Индекс крутизны. [13] |
Понятие индекса крутизны представляется наиболее полезным в связи с концентрационно-логарифмической диаграммой, так как величина ц для любой точки эквивалентности может быть приближенно получена из диаграммы. [14]
Вычисление рН многих подобных сложных систем существенно упрощается при использовании концентрационно-логарифмических диаграмм. Наклон кривой диссоциации многоосновной кислоты связан простым соотношением с буферной емкостью смеси их солей. Выведем некоторые общие зависимости буферной емкости смеси от рН, но вначале рассмотрим некоторые характерные примеры. [15]
Страницы: 1 2
