Масса - катод
Cтраница 3
При проведении опыта по определению электрохимического эквивалента меди были получены следующие данные: время прохождения тока t - 20 мин, сила тока / - 0 5 А, масса катода до опыта ml 70 4 г, масса катода после опыта т2 70 52 г. Какое значение электрохимического эквивалента меди было получено по этим данным. [31]
 |
Катоды косвенного накала. [32] |
Достоинством ламп с катодами косвенного накала, кроме того, является незначительный микрофонный эффект. Масса катода сравнительно велика, и его трудно привести в состояние колебаний. [33]
При прохождении постоянного электрического тока через кулонометр происходит растворение серебра на аноде и его осаждение на катоде. По изменению массы катода определяют количество прошедшего электричества. [34]
Через раствор, содержащий ионы Си2, в течение 5 00 мин пропускают ток постоянной силы. За это время масса катода увеличивается на 1 24 г. Какова сила пропускаемого тока в амперах. [35]
Время наращивания полновесного катода в товарных ваннах на различных заводах колеблется от 6 до 15 сут. Ко времени выгрузки масса катода достигает 60 - 140 кг. После тщательной промывки готовые катоды направляют потребителю или переплавляют в слитки. [36]
В процессе электролиза масса катода медного кулонометра увеличилась на 0 48 г, а массы катодов второго и третьего кулонометров-соответственно на 0 84 и 1 62 г. Определить, из каких металлов изготовлены электроды во втором и третьем кулонометрах. [37]
Количественное осаждение элемента при электрогравиметрическом анализе достигается за счет пропускания большого избытка тока. Количество выделившегося осадка определяют по массе катода до и после электролиза. Иногда определение основано на измерении массы осадка окисла металла, образовавшегося на аноде. [38]
Приходной статьей баланса тока является количество электричества, прошедшее через электролизер. Оно определяется расчетным путем по массе катода кулонометра. [39]
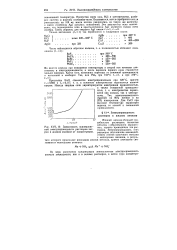 |
Зависимость эквивалентной электропроводности растворов натрия в жидком аммиаке от концентрации. [40] |
Пропустив через соль 96 5 к электричества, разберем систему и взвесим составные части. Оказывается, масса серебряного анода уменьшилась на 108 мг, масса катода увеличилась на такую же величину, а масса столбиков AgJ осталась неизменной. Эти результаты ясно показывают, что переносчиком тока в кристаллическом AgJ являются только ионы серебра. [41]
При электролизе в растворах солей масса катода увеличивается, так как на катоде осаждаются положительные ионы. Например, если электролитом является раствор медного купороса и мы берем медные электроды, то масса катода увеличивается со временем. [42]
Простейший электрохимический кулонометр позволяет определить суммарное количество электричества, прошедшего в цепи за данное время, либо по увеличению массы катода, включенного последовательно в цепь электролитической ячейки, либо по изменению рН раствора, либо по объему выделившегося газа. Метод требует дополнительных операций и не позволяет считывать результат непосредственно со шкалы прибора. Более совершенными являются приборы с хемотронными преобразователями ( электрохимическими интеграторами), включенными в качестве датчика в электронную измерительную цепочку. [43]
 |
Данные аналитических определений п расчетные величины. [44] |
Во время электролиза контролируют содержание Б растворе манганата и перманганата. С этой целью через каждые 20 - 30 мин на некоторое время отключают ток, отбирают для анализа пробу электролита и определяют изменение массы катода кулонометра. [45]
Страницы: 1 2 3 4