Масса - моль
Cтраница 3
То, что химики называют молекулярным весом, есть не что иное, как масса моля молекул в граммах. [31]
На нейтрализацию Н3РО4 массой 0 943 г израсходовано КОН массой 1 291 г. Вычислите массу моля эквивалентов кислоты. [32]
Плотность воды р равна 1000 кг / м3 ( 1 г / см3), масса моля [ л, 18 - Ю 3 кг / моль. [33]
Плотность воды р равна 1000 кг / м3 ( 1 г / см3), масса моля JA 18 - 10 - 3 кг / моль. [34]
Изменение массы на моль образовавшегося водорода составит 4 3 - 10 - 9 г; масса моля водорода известна с точностью до 10 - 8 г; следовательно, современными средствами обнаружить такое изменение массы невозможно даже в приведенном примере самой выгодной в энергетическом отношении химической реакции; тем более это невозможно в других случаях. [35]
Для вычисления концентрации насыщенного раствора электролита в граммах на литр нужно умножить количество молей на массу моля данного соединения. [36]
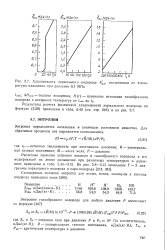 |
Хладоемкость нормального водорода hfnjp отсчитанная от тгмпе-ратуры плавления при давлении 0 1 МПа. [37] |
Ср - истинная теплоемкость при постоянном давлении; К - универсальная газовая постоянная; М - масса моля; Р - давление. [38]
Следствие из закона Авогадро: М: Mz m: niz, где MI и MZ - масса молей двух газов, т и т2 - массы одинаковых объемов этих газов, измеренные в одинаковых условиях. [39]
Теплоемкость, отнесенная к 1 г вещества, называется удельной, к массе атома - атомной и к массе моля - молярной теплоемкостью. [40]
Готовят нормальные растворы аналогично молярным с той лишь разницей, что при определении массы растворяемого вещества нужно брать не массу моля, а массу грамм-эквивалента. [41]
Зная массу гидрофосфата аммония ( 66 г), образовавшегося в результате реакции ( 3), и обозначив массу моля исходного неизвестного металла через х, на основании уравнений реакций ( 1) - ( 3) можно определить неизвестный металл. Так как в результате расчетов атомная масса исходного металла оказывается равной 65 г, то очевидно, что металл является цинком. [42]
Число атомов в единице объема равно ( / M) NA, где б - плотность металла, М - масса моля, NA - число Авогадро. [43]
Высокомолекулярными соединениями ( ВС), или полимерами, называются соединения, молекулы которых содержат тысячи и десятки тысяч атомов, масса моля этих соединений составляет сотни тысяч и даже миллионы. [44]
Число атомов в единице объема равно ( б / М) / VA где 6 - плот-но - Th металла, М - масса моля, VA число Авогадро. [45]
Страницы: 1 2 3 4