Масса - полученный продукт
Cтраница 1
Масса полученного продукта составляет 90 - 93 г. При упаривании маточного раствора в вакууме до 25 мл, после обесцвечивания раствора активированным углем и охлаждения до 0 удается получить еще небольшое количество вещества. [1]
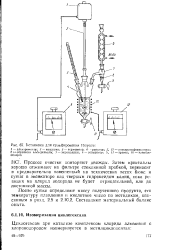 |
Остановка для сульфировании толуола. [2] |
Поело сушки определяют массу полученного продукта, его температуру плавления и кислотное число по методикам, описанным п разд. Составляют материальный баланс опыта. [3]
Выход готового продукта определяется как отношение массы полученного продукта к массе сырья, затраченного на его производство. [4]
Промытую лепешку переносят во взвешенную колбу или кубик для отгона растворителя и после отгона определяют массу полученного продукта ( парафина-или церезина-сырца) и его выход от исходного сырья. Фильтраты и промывки первой и второй ступеней обезмасливания сливают во взвешенную колбу или кубик для отгона растворителя, после отгона определяют количество ( выход) отходов обезмасливаиия. Полученные продукты анализируют, определяя температуру плавления на шарике термометра, содержание масла экспресс-методом ( ГОСТ 9090 - 59) и глубину проникания иглы при 25 С. [5]
Водно-спиртовой раствор алкилсульфатов ( нижний слой) вылавливают в предварительно взвешенную на технических весах фарфоровую чашку и при периодическом перемешивании стеклянной палочкой упаривают на кипящей водяной бане до образований густой пасты; определяют массу полученного продукта. [6]
Каждое химическое уравнение символизирует собой закон сохранения массы. Левая часть уравнения выражает массу исходных, а правая - - массу полученных продуктов реакции. Известно, что в химических реакциях сохраняется не только масса реагирующей системы, но и ее энергия. Таким образом, химическое уравнение символизирует собой также и закон сохранения энергии в химических реакциях. [7]
Если протекающий химический процесс описывается стехиометрическим уравнением, то выход продукта находят как отношение массы полученного продукта к теоретически возможному. [8]
Количественно электрохимические процессы описываются законами Фарадея. Эффективность электролиза характеризуется такими факторами, как сила и плотность тока, напряжение, выход по току и веществу, расход электроэнергии на единицу массы полученного продукта. Особенность электрохимических методов заключается в селективности, зависящей от потенциала электрода. [9]
Принципиальное отличие заключается в том, что выходящее из цикла в природе вещество не является ксенобиотиком, не представляет собой загрязнения и уходит не в отход, а в запас. Понятно также, что полностью уподобить ресурсный цикл естественному биогеохимическому циклу невозможно. Закон сохранения вещества с очевидностью показывает, что безотходная технология в принципе невозможна, и в общем случае под ней следует понимать идеальное и теоретически недостижимое сочетание технологических процессов, в которых масса полученных продуктов равна массе израсходованных сырьевых и прочих материалов. [10]
Ми ж ний слой ( раствор солей) сливают в делительную воронку из термостойкого стекла и охлаждают на водяной бане с температурой 5 С до тех пор, пока ие произойдет четкое расслоение раствора солен. При этом сульфонаты натр л я собираются в В t р х н с м к л се подобием слое. Нижний слой ( чзодный раствор хлорида натрия) сливают, а сульфо-лзты натрия, оставшиеся в делительной воронке, разбавляют половиной объема 50 % го этанола и оставляют стоять для выделения неомыленных веществ, оставшихся после первого расслаивания. Вновь образовавшийся нижний слой - сульфонаты натрия - - сличают е предварительно взвешенную фарфоровую чашку, выпаривают па кипящей водяной бане до консистенции пасты и определяют массу полученного продукта. [11]
Страницы: 1