Активная масса - электрод
Cтраница 2
 |
Электрохимические процессы кислотного аккумулятора. а - при разряде, б - при заряде. [16] |
Теоретически аккумулятор может разряжаться до полного превращения активных масс электродов в сернокислый свинец. Однако практически разряд прекращают гораздо раньше. Получающийся при разряде сернокислый свинец представляет собой соль белого цвета, плохо растворяющуюся в электролите и обладающую низкой электропроводностью. Поэтому разряд ведут не до конца, а только до того момента, когда напряжение аккумулятора снижается до 1 7 - 1 8 В. [17]
Аккумулятор может разряжаться теоретически до полного превращения активных масс электродов в сернокислый свинец и истощения электролита. Однако практически разряд прекращают гораздо раньше. Образующийся при разряде сернокислый свинец представляет собой соль белого цвета, плохо растворяющуюся в электролите и обладающую низкой электропроводностью. Поэтому разряд ведут не до конца, а только до того момента, когда в сернокислый свинец перейдет около 35 % активной массы. В этом случае образовавшийся сернокислый свинец равномерно распределяется в виде мельчайших кристалликов в оставшейся активной массе, которая сохраняет еще достаточную электропроводность, чтобы обеспечить напряжение между электродами 1 7 - 1 8 В. [18]
Аккумулятор может разряжаться теоретически до полного превращения активных масс электродов в сернокислый свинец и истощения электролита. Однако практически разряд прекращают гораздо раньше. Образующийся при разряде сернокислый свинец представляет собой соль белого цвета, плохо растворяющуюся в электролите и обладающую низкой электропроводностью. Поэтому разряд ведут не до конца, а только до того момента, когда в сернокислый свинец перейдет около 35 % активной массы. [19]
При уравнительном заряде преследуется цель полностью обеспечить восстановление активных масс электродов всех аккумуляторов батареи. Как правило, потребность в уравнительном заряде возникает у батарей после длительной эксплуатации, когда в батареях появляются аккумуляторы с повышенной степенью разряженности. [20]
Диоксид марганца находит широкое применение в качестве компонента активной массы электродов гальванических элементов, как окислитель, абсорбент и катализатор. Перманганат калия используют как окислитель в органическом синтезе, а антисептическое действие его находит применение в медицине. [21]
 |
Ячейка и схема для поляризационных измерений. [22] |
Oz [2, 5], их адсорбция из газовой фазы каталитически активной массой электрода происходит со значительной скоростью и не влияет на кинетику электрохимического процесса. Кроме того, такой способ подачи позволяет расширить температурный диапазон исследований, ограниченный ранее низкой температурой кипения большинства электрохимически активных органических соединений или образующихся азеотропов, в связи с чем возможно более точное определение кинетических параметров изучаемого процесса. [23]
Увеличенный саморазряд вызывается присутствием примесей в электролите и в активных массах электродов, а также наличием коротких замыканий во внутренней и внешней цепи. [24]
Необходима периодическая подзарядка бездействующих АБ во избежание необратимых изменений состава активной массы электродов. Саморазряд возникает вследствие нескольких причин, главные из которых - химическое взаимодействие электролита с пластинами электродов; самопроизвольное преобразование компонентов активной массы пластин; наличие градиента плотности электролига вдоль нысоты электрода. Последнее обусловливает неэквипотенциальность электрода по высоте: более высокий потенциал имеет место в нижней части пластин, где плотность электролита увеличена, что приводит к возникновению уравнительного тока внутри АБ. [25]
Необходимо помнить, что все описанные процессы происходят на границе раздела активной массы электрода и электролита. Наприме ( р, переход губчатого свинца в сульфат свинца происходит на поверхности кристаллов металлического свинца, а1 так как сульфат свинца весьма слабо растворим в растворах серной кислоты, то он при своем образовании тотчас образует пересыщенный раствор, из которого выпадают мелкие кристаллы, размещаясь в пространстве, занятом до этого кристаллами металлического свинца. [26]
Значение динамической ЭДС зависит от плотности электролита, непосредственно соприкасающегося с активной массой электродов, степени расхода активных масс и не зависит от размеров пластин. При разряде и заряде аккумулятора эта ЭДС непрерывно меняется. [27]
Работы в области свинцовых аккумуляторов были направлены главным образом на исследование структуры активных масс электродов этих аккумуляторов и на сохранение структуры при длительной эксплуатации их в различных режимах. [28]
При заряде реакция идет в обратном направлении и, следовательно, происходит восстановление активной массы электродов. При заряде и разряде концентрация электролита остается неизменной. [29]
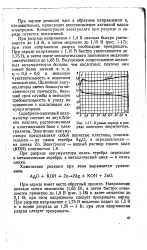 |
Кривые заряда и разряда щелочного аккумулятора. [30] |
Страницы: 1 2 3 4