Эквивалентная масса - соль
Cтраница 1
Эквивалентная масса соли равна ее мольной массе, деленной на произведение валентности металла на число его атомов в молекуле. [1]
Эквивалентная масса соли равна частному от деления ее молярной массы на произведение числа конов металла и его валентности. [2]
Эквивалентная масса соли равна ее мольной массе, деленной на произведение валентности металла на число его атомов в молекуле. В зависимости от характера реакции она может иметь различное значение. Например, мольная масса NaCl равна 58 44 г / моль, эквивалентная масса 58 44: 1 58 44 г / моль. У NaHSO4 могут быть 2 значения эквивалентной массы: мольная масса - 120 г / моль, эквивалентная масса 120: 1 120 г / моль и 120: 2 60 г / моль. Понятие эквивалентной массы особенно важно в количественном анализе. [3]
Находим эквивалентную массу соли: NaHSO4 NaHSO. [4]
Находим эквивалентную массу соли: NaHSO4 маНЗоУ / 1 120 г / моль. [5]
Находим эквивалентную массу соли: 5NaHSO4 MNaHSO4 / l 120 г / моль. [6]
Находим эквивалентную массу соли: Эыанзо, А1ианзо / 1 120 г / моль. [7]
При расчете эквивалентной массы солей железа ( II), вступающих во взаимодействие с перманганатом, видим, что каждая молекула FeSO4, окисляясь, отдает один электрон, а поэтому ее эквивалентная масса будет равна 151 9 г / моль. [8]
В качестве примера приведена табл. 15 эквивалентных масс солей жесткости. [9]
В качестве примера приведена табл. 15 эквивалентных масс солей жесткости. [10]
Так как по уравнению реакции вместо сильной кислоты НА образуется эквивалентная масса соли ВА, концентрация раствора не меняется. [11]
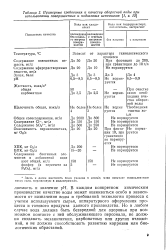 |
Примерные требования к качеству оборотной воды при использовании поверхностных и подземных источников [ 1, с. 13 ]. [12] |
Здесь и далее жесткость воды указана в мэкв / л; мэкв означает эквивалентную массу соли, выраженную в миллиграммах. [13]
Поскольку Ре2 - ион, переходя в Ре3 - ион, повышает степень окисления на единицу, то эквивалентная масса соли Мора совпадает с мольной массой. [14]
Эквивалентная масса кислоты ( эквивалент кислоты) равна ее молекулярной массе, деленной на число атомов водорода, замещаемых в данной реакции. Эквивалентная масса основания ( эквивалент основания) равна молекулярной массе основания, деленной на число гидроксильных групп, замещаемых в данной реакции. Эквивалентная масса соли ( эквивалент соли по металлу) равна молекулярной массе соли, деленной на произведение числа атомов металла и валентного состояния металла. [15]
Страницы: 1