Атомная масса - металл
Cтраница 3
Определяющее значение для нахождения относительных атомных масс имело уточнение понятий атома, молекулы и эквивалента, сделанное соотечественником Аво-гадро Станислав Канниццаро в 1858 г. в статье Краткое изложение курса химической философии, а также предложенный Канниццаро способ определения атомных масс металлов с использованием их атомных теплоем-костей. [31]
Оценка приведенных результатов теоретических и экспериментальных исследований по степени взаимодействия в карбидно-окисных системах МегС - МеО позволяет с некоторым приближением сделать вывод о том, что в ряду карбидных соединений ( в сочетании с одним окислом) реакционность систем уменьшается по группам с увеличением атомной массы металла карбидного соединения и возрастает при переходе от карбидов металлов IV группы к карбидам металлов V и VI групп. [32]
Кь Кг - константы, относящиеся к осаждению металла; т ] - перенапряжение выделения металла; ( 100 - as) - поверхность, реально используемая для осаждения металла; Кз, К4 - константы, характеризующие адгезию частиц к поверхности, и процесс их соосаждения; А - атомная масса металла матрицы; t - плотность тока; п - заряд иона разряжаемого металла; F - константа Фарадея; р - плотность металла матрицы. [33]
При нормальных условиях 1 540 г металла вытесняют из кислоты 0 617 л водорода. Вычислите атомную массу металла и назови те его. [34]
При нагревании в кислороде 0 2774 г металла получено 0 2988 г его оксида. Определите атомную массу металла, если степень окисления его равна двум, и составьте формулу оксида. [35]
При взаимодействии с водой металла, степень окисления которого 2, выделяется 500 мл водорода. Чему равна атомная масса металла. Как называется этот металл. [36]
При пропускании тока силой 2А в течение 1 ч 14 мин 24 с через водный раствор хлорида металла ( II) на одном из графитовых электродов выделилось 2 94 г металла. Чему равна атомная масса металла, если выход потоку 100 %, и что это за металл. [37]
Электрический ток силой в 6 а в течение 1 ч 14 мин 24 сек осадил на катоде 8 14 г металла из химического соединения, в котором он двухвалентен. Чему равна атомная масса металла и какой это металл. [38]
На восстановление 9 9375 г оксида двухвалентного металла израсходовано 0 25 г водорода. Чему равны эквиваленты оксида и металла, атомная масса металла. [39]
В действительности теплоемкости получаемых металлов несколько отличаются. Соотношение между массой металла и оксида алюминия меняется в зависимости от состава исходного оксида и атомной массы металла. Тепловые потери также меняются. При большом количестве шихты они меньше, а когда берут небольшие массы веществ ( в лабораторных опытах), они больше. [40]
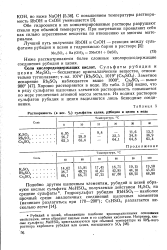 |
Растворимость ( в вес. % сульфатов калия, рубидия и цезия в воде. [41] |
Хорошо растворяются в воде. Из табл. 5 [35] видно, что в ряду сульфатов щелочных элементов растворимость повышается по мере увеличения атомной массы металла. Из водных растворов сульфатов рубидия и цезия выделяются лишь безводные соединения. [42]
Учитывая, что полученный для опыта металл переходит при реакции с кислотой в степень окисления - - 2 или - f - З, найдите возможные значения атомной массы металла и определите, какой это металл. [43]
Метод Канниццаро позволял находить атомные массы только тех элементов, которые входят в состав газообразных или легко переходящих в газообразное состояние соединений. Большинство же металлов не образует таких соединений. Поэтому при определении атомных масс металлов в свое время был использован другой метод, основанный на зависимости между атомной массой элемента и удельной теплоемкостью соответствующего простого вещества в твердом состоянии. [44]
Метод Канниццаро позволял находить атомные массы толькс тех элементов, которые входят в состав газообразных или легко переходящих в газообразное состояние соединений. Большинство же металлов не образует таких соединений. Поэтому при определение атомных масс металлов в свое время был использован другой метод, основанный на зависимости между атомной массой элемента и удельной теплоемкостью соответствующего простого вещества в твердом состоянии. [45]
Страницы: 1 2 3 4