Атомная масса - химический элемент
Cтраница 1
Атомная масса химического элемента - средняя масса смеси изотопов; она хотя и растет с ростом заряда ядра, но не всегда, так как в смеси иногда оказывается особенно много легких изотопов. Именно по этой причине средняя атомная масса элементов ( элементная масса) калия, никеля, иода и протактиния оказалась меньше, чем у аргона, кобальта, теллура и тория. [1]
Основные научные работы посвящены определению атомных масс химических элементов. [2]
Плотность кристалла ионного типа зависит от атомной массы химических элементов, входящих, в его состав, и от структуры. [3]
Большое значение имело предпринятое на основе периодического закона исправление атомных масс химических элементов. [4]
Таким образом, применение закона Авогадро, а также следствий из него для определения атомных масс химических элементов и установления химических формул многих соединений не представляет больших трудностей. [5]
Свойства простых веществ, а также свойства и формы соединений находятся в периодической зависимости от атомных масс химических элементов. [6]
Свойства простых веществ, а также свойства и формы соединений находятся в периодической зависимости от величины атомных масс химических элементов. [7]
Химические элементы, существующие в природе, представляют собой смеси изотопов. Поэтому атомная масса химического элемента представляет собой среднее значение атомных масс всех его изотопов. [8]
Дальтона, были заняты определением точных атомных масс химических элементов. [9]
Его заслуга особенно велика в точном определении атомных масс химических элементов. Исходя из того, что неорганические соединения элементов с водородом встречаются сравнительно редко, а с кислородом соединяются почти все элементы, атомные массы элементов Берцелиус вычисляет по отношению к кислороду. [10]
 |
Кристаллические решетки алмаза а и графита б. [11] |
Дальтон, не имея средств для измерения абсолютной массы атомов, принял атомную массу наиболее легкого элемента водорода за единицу и с ней сравнивал атомные массы других элементов. Дальтону, атомная масса химического элемента представляется относительным числом, показывающим, во сколько раз атом данного элемента тяжелее атома водорода. [12]
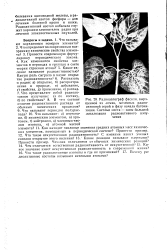 |
Радиоавтограф фасоли, выращенной из - семян, меченных радиоактивной серой в фазу начала бутонизации. Светлые места - зоны большой локализации радиоактивного излучения. [13] |
Что называют периодом полураспада. Что называют: а) изотопами, б) химическим элементом, в) протоном, г) нейтроном, д) массовым числом изотопа, е) атомной массой элемента. Как находят числовые значения средних атомных масс химических элементов, помещаемых в периодической системе. [14]
Основные научные исследования посвящены определению атомных масс химических элементов. [15]
Страницы: 1 2