Массы - молекула
Cтраница 1
Массы молекул сосредоточены в этих точках. [1]
Массы молекул и атомов также чрезвычайно малы. [2]
Массы молекул, атомов и элементарных частиц измеряют в углеродных единицах ( у. Эта единица, равная 1 / 12 массы атома углерода С, введена в 1961 г. в соответствии с международным соглашением. [3]
Массы молекул и атомов также чрезвычайно малы. [4]
Когда массы молекул равны ( mt m2), то v c v c и f2c ic так что общим результатом столкновения является обмен компонентами скорости, направленными вдоль линии центров. Когда массы сильно различны. [5]
Если массы молекул равны и А ( 11А2), то термодиффузия отсутствует. Коэффициенты диффузии обратно пропорциональны давлению. [6]
Когда массы молекул равны ( mi пг2), то v c v c и v 2c VIE, так что общим результатом столкновения является обмен компонентами скорости, направленными вдоль линии центров. [7]
Следовательно, массы молекул одного и того же вещества, находящихся в разных стационарных состояниях, различны и поэтому масса тела ( системы) не пропорциональна числу молекул. Отсюда следует вывод о том, что количество вещества есть величина, принципиально отличная от массы. [8]
Как она зависит от массы молекул и их скорости. [9]
Как она зависит от массы молекул и их скорости. [10]
Закон Авогадро позволил определить массы молекул и атомов только для простых газообразных веществ. Однако на его основе Станислав Канниццаро создал метод расчета атомных масс элементов, которые сами не являются газообразными, но образуют несколько летучих соединений. Идея метода проста: в молекуле не может быть менее одного атома. Следовательно, атомная масса элемента равна наименьшей его доле в различных соединениях. [11]
Зависит ли эта доля от массы молекул и температуры. [12]
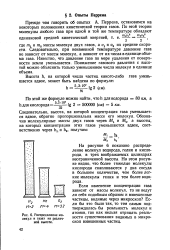 |
Распределение молекул в газах на различной высоте. [13] |
Если изменение концентрации газа зависит от массы молекул, то не ведут ли себя подобным образом и взвешенные частицы, видимые через микроскоп. [14]
Это выражение не зависит явно от массы молекулы, поскольку поступательные статистические суммы начального и активированного состояний сокращаются. Отношение чисел симметрии обычно не может сильно отличаться от единицы. Из трех главных моментов инерции при растяжении разрываемой связи, как правило, может заметно возрастать только один, например, А. [15]
Страницы: 1 2 3 4