Медленность
Cтраница 2
Медленность установления ионизационного равновесия в данном случае объясняется малой плотностью оболочки. [16]
Медленность установления фазовых равновесий приводит к отклонениям от равновесия вследствие изменения условий ( давления и температуры) в различных процессах добычи нефти. Изменение условий сопровождается изменением равновесного состояния. [17]
Медленность стадии образования молекул водорода из атомов приводит к повышению концентрации адсорбированного атомарного водорода на поверхности металла, которая легко может быть обнаружена по замедлению спада потенциала после размыкания поляризующего тока, как это наблюдалось, например, П. Д. Луковцевым и С. Д. Левиной [ 35J для случая никеля в щелочных растворах. Существенные данные о медленности стадий, следующих за стадией разряда, получаются также при наблюдении проникновения водорода внутрь металла. Задержки в удалении адсорбированного водорода, приводящие к повышению его концентрации на поверхности, приводят также к усилению его диффузии в металл. [18]
Эта медленность позволяет писать уравнения Максвелла для полей каждой из основных частот в отдельности. [19]
Эта медленность позволяет писать уравнения Маклвелла для полей каждой из основных частот в отдельности. [20]
Эта медленность позволяет писать уравнения Маклвелла для полей каждой из основных частот в отдельности. [21]
Известна медленность и необратимость реакций окисления с участием молекулярного кислорода. Имеется много данных о том, что в присутствии ионов водорода кислород, как правило, восстанавливается с образованием перекиси водорода. [22]
Благодаря медленности, с которой устанавливается ионное равновесие в кристаллическом кварце, нам с А. [23]
Однако медленность и малая высота подъема делают нецелесообразным их применение при небольшом ( до 10 т) весе деталей. [24]
Благодаря медленности, с которой устанавливается ионное равновесие в кристаллическом кварце, нам с А. А. Шапошниковым удалось в выражении для электропроводности с разделить влияние концентрации ионов Nn от влияния подвижности ии. [25]
Выражая медленность реакции с помощью величин, имеющих размерность энтропии, мы тем самым лишь иначе формулируем проблему, но отнюдь не решаем ее. [26]
Вследствие медленности сочетания диазотированной аминосали-циловой кислоты, а также по другим причинам, более удобным является использовать соединения, в которых аминогруппа и остаток салициловой кислоты разделены какими-либо группами. [27]
Учитывая медленность движения ( TO - 10 - 12 сек), рассмотрение ведется в классическом приближении. [28]
Вследствие медленности окисления не было замечено хемолюминесценции при пропускании кислорода в темноте. [29]
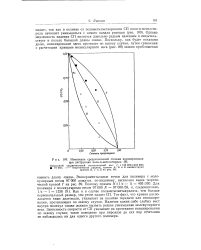 |
Изменение среднечисловой степени полимеризации при деструкции поли-а-метилстирола. [30] |
Страницы: 1 2 3 4