Медленность - установление - равновесие
Cтраница 1
 |
Зависимость величины адсорбции I - г - от v so. [1] |
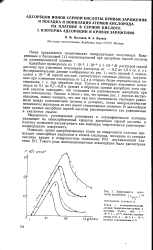
Медленность установления равновесия и логарифмическая изотерма указывают на хемосорбционный характер адсорбции серной кислоты, а платину позволяют рассматривать как имеющую энергетически равномерно-неоднородную поверхность. [2]
Медленность установления равновесия в системе, состояние ко торой близко к критическому, порождает явление, называемое гистерезисом плотности. [3]
Ввиду чрезвычайной медленности установления равновесия и незначительности давлений эти данные мало точны, и теплота диссоциации не может быть вычислена. [4]
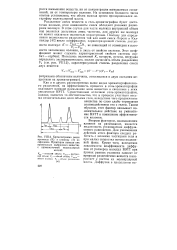 |
Хроматограмма смеси крахмала ( К и глюкозы ( Г на сефадексе. Пунктиром нанесен пик произвольно выбранного вещества с промежуточной молекулярной массой. [5] |
Вторым фактором, оказывающим влияние на размывание, является медленность установления диффузионного равновесия. Для уменьшения действия этого фактора следует работать с мелкими частицами геля и при малых скоростях потока подвижной фазы. Кроме того, вследствие зависимости коэффициента диффузии от размеров молекул ВЭТТ при прочих равных условиях зависит от природы разделяемых веществ и возрастает с ростом их молекулярной массы. [6]
Как указывалось выше, вторая группа факторов, приводящих к размыванию полосы, связана с медленностью установления равновесия. [7]
Таким образом, в случае адсорбции на цеолитах ряда нормальных алканов с достаточно большим молекулярным весом при газохроматографи-ческих определениях существенную роль начинает играть медленность установления равновесия за счет внутренней диффузии в каналах пористых кристаллов цеолитов. [8]
 |
Диаграмм образования молекулярный водородом вращательной полосы в спектре Лайманя. [9] |
Сохранение в жидком водороде отношения интенсивностей линий 3: 1 указывает, как говорилось выше, на то, что нормальное соотношение обеих форм сохраняется при низких температурах вследствие медленности установления равновесия. При выдерживании водорода в жидком виде в течение некоторого времени увеличивается интенсивность линий, соответствующих переходу 0 - 2 для пара-молекул; следовательно, идет самопроизвольное орто-пара-превра-щение. После достижения равновесия почти все молекулы должны занимать самый низкий уровень ( / 0) и весь водород будет почти исключительно в пара-форме. [10]
Предполагается, что медленные состояния локализуются на внешней поверхности окисной пленки. Медленность установления равновесия их с объемом полупроводника обусловлена тем, что для прохождения электронов сквозь окисный слой, являющийся изолятором, требуется значительное время. С увеличением толщины окисной пленки постоянная времени увеличивается. [11]
Теоретически из-за сдвига равновесия при электрорастворении металла из амальгамы в анодном процессе твердая фаза должна оказывать влияние на электродный процесс. Но практически из-за медленности установления равновесия между твердой фазой и раствором металла в ртути наличие осадка металла обычно не оказывает заметного влияния на высоту анодного пика. [12]
Конечность скорости сорбции и десорбции должна приводить к такому же симметричному размыванию полосы для случая линейной изотермы, как и диффузионные процессы. При отсутствии потока медленность установления равновесия не вызывает изменения формы полосы. [13]
Это, очевидно, и может служить объяснением тех расхождений, которые возникают в результате исследований статическим и динамическим методами. В первом случае, вследствие медленности установления равновесия, одновременно протекает и процесс старения, в результате которого получается устойчивая форма окиси магния с характерной для нее структурой периклаза. Во втором случае, при быстром течении процесса, образовавшаяся окись магния еще не успевает приобрести устойчивую структуру, сохраняя решетку брусита. [14]
Частичный гидролиз HBF4 с образованием разлагаемого щелочью BF3OH объясняет безуспешность попыток [161, 162] определения концентрации кислоты путем непосредственного титрования щелочью. Зависимость равновесного состава от температуры и концентрации раствора и медленность установления равновесия приводят к отмеченной [161 ] зависимости результатов титрования от разбавления, температуры и длительности стояния раствора. Данные [162] грубо ошибочны, так как авторы полагали, что им удается оттитровать BF, и их рекомендации не заслуживают внимания. [15]
Страницы: 1 2