Выделяющаяся медь
Cтраница 1
Выделяющаяся медь оседает на железной пластинке. [1]
Выделяющаяся медь осаждается на железной пластинке. Из уравнения ( 2) следует, что количество переходящего в раствор железа ( в виде ионов Fe2) равно количеству осаждающейся на пластинке металлической меди. [2]
Выделяющаяся медь не мешает дальнейшему ходу определения. Также не оказывает влияния и небольшое содержание марганца в магниевых сплавах. Затем приливают к растворенной пробе ровно столько раствора желе-зистосинеродистого калия, чтобы связать почти весь цинк. После этого выжидают не менее 15 минут и тогда только начинают прибавлять по 0 5 мл раствора железистосинеродистого калия, всякий раз делая капельную пробу, причем между прибавлением каждой небольшой порции раствора железистосинеродистого калия и капельной пробой должно проходить не менее 15 минут. Если производить титрование точно по описанию, то переход окраски в капельной пробе бывает достаточно резким и метод дает сходящиеся результаты. [3]
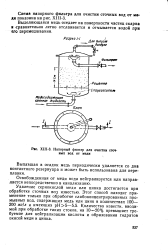 |
Напорный фильтр для очистки сточных вод от меди. [4] |
Выделяющаяся медь оседает на поверхности частиц скарпа сравнительно легко отслаивается и отмывается водой при его перемешивании. [5]
Качество получаемых пленок недостаточно высокое ввиду того, что при термическом разложении, наряду с выделяющейся медью, образуются побочные продукты в результате пиролиза ацетилацетонатной группы. В дальнейшем они могут распадаться с выделением углерода, который загрязняет пленку, ухудшает ее механические свойства и смачиваемость припоями. Поверхность пленки становится шероховатой, а электросопротивление ее повышается. [6]
Поэтому при проведении этой реакции окись меди - щужно нагреть лишь до начала реакции; далее она продолжается и при отставленной горел-ке самопроизвольно и сопровождается самораскаливанием докрасна выделяющейся меди. Реакция восстановления окиси меди практически необратима. Совершенно иное получается при восстановлении водородом окислов железа. [7]
При электролитическом методе определения меди требуется получение прозрачного раствора, свободного от мышьяка, сурьмы, олова, молибдена, золота, платиновых металлов, серебра, ртути, висмута, селена ( IV) и теллура ( IV), загрязняющих осадок выделяющейся меди. Кроме того, должны отсутствовать: роданистоводородная кислота, присутствие кото-р Ьй делает осадок меди губчатым, и соляная кислота, действующая аналогично и, кроме того, вызывающая растворение платины на аноде и переход ее на катод. Электролиз может быть проведен в азотнокислом или сернокислом растворе, и обычно его проводят в смеси обеих кислот. Если применяется одна азотная кислота, имеется опасность замедленного или неполного осаждения. Катод и анод желательно иметь в виде открытых сетчатых платиновых цилиндров с матированной поверхностью, полученной при помощи пескоструйного аппарата ( стр. [8]
При электролитическом методе определения меди требуется получение прозрачного раствора, свободного от мышьяка, сурьмы, олова, молибдена, золота, платиновых металлов, серебра, ртути, висмута, селена ( IV) и теллура ( IV), загрязняющих осадок выделяющейся меди. Кроме того, должны отсутствовать: роданистоводородная кислота, присутствие которой делает осадок меди губчатым, и соляная кислота, действующая аналогично и, кроме того, вызывающая растворение платины на аноде и переход ее на катод. Электролиз может быть проведен в азотнокислом или сернокислом растворе, и обычно его проводят в смеси обеих кислот. Если применяется одна азотная кислота, имеется опасность замедленного или неполного осаждения. [9]
Однако при практически применяемых плотностях тока выход по току в медноцианистых электролитах значительно ниже, чем в кислых. Кроме того, выход по току в цианистых электролитах с повышением DK резко уменьшается, и при равных значениях DK количество выделяющейся меди на катоде в кислых и цианистых электролитах практически одинаково. Основным побочным электрохимическим процессом на катоде при выделении меди является разряд ионов водорода. [10]
При взаимодействии с растворами солей меди железо восстанавливает ион меди до металла. В пробирку с раствором сернокислой меди опускают железный гвоздь или кусок железной проволоки, гвоздь и проволоку нужно тщательно зачистить наждачной бумагой. Вскоре можно наблюдать изменение цвета железа: выделяющаяся медь откладывается на железе тонким слоем. [11]
При взаимодействии с растворами солей меди железо восстанавливает ион меди до металла. В пробирку с раствором сульфата меди опускают железный гвоздь или кусок железной проволоки, предварительно тщательно зачистив их наждачной бумагой. Вскоре можно наблюдать изменение цвета железа; выделяющаяся медь откладывается на железе тонким слоем. [12]
Кезеги и Киш [37] усовершенствовали медносульфат-ный метод. Для анализа авторы берут отмеренное количество раствора сернокислой меди и избыток ее после растворения Ремет определяют йодометрически. Навеску обрабатывают раствором сернокислой меди в течение 15 мин на водяной бане при 95 - 100 С. Стогний и Кириленко [38] применили для растворения Ремет раствор сернокислой меди, содержащий сернокислый калий, что предотвращает частичное растворение закиси железа. Медь отделяют от окислов железа растворением в растворе углекислого аммония в присутствии кислорода воздуха. Ртуть амальгамирует выделяющуюся медь, поэтому она не закрывает поверхность частиц Ремет и не мешает его растворению. [13]
Страницы: 1