Восстановленная медь
Cтраница 3
Рессель и Г Иринг нашли, что скорость гидрирования этилена на восстановленной меди заметно не изменяется в присутствии закиси азота, но что скорость образования этана быстро уменьшается, как только адсорбированная закись азота начинает разлагаться с образованием окисной пленки на поверхности меди. Эти авторы пришли к заключению, что участки поверхности, активные в отношении образования этана, являются также наиболее активными и в отношении разложения закиси азота. [31]
 |
Упругость пара третичного бутилового спирта. [32] |
Окисление можно осуществить с помощью серебряного катализатора, а дегидрогенизацию в присутствии восстановленной меди; были также успешно применены для обеих реакций и другие катализаторы. Так Ottensooser28 каталитическим окислением воздухом при 335 - 340 над окисью цинка превратил в соответствующий кетой 93 % вторичного бутилового спирта. В качестве промышленного способа было предложено проводить смесь воздуха и паров спирта над катализатором, нагретым по крайней мере до 500; при этом для поддержания нужной температуры достаточно теплоты реакции. В качестве катализатора была предложена медь2в или в чистом виде, или с примесью других металлов, например цинка. [33]
Установлено, что при соблюдении указанных условий сожжения нет необходимости в применении восстановленной меди, функцию которой выполняют сами продукты разложения органического вещества. [34]
Ипатьев утверждает, что гидрогенизация лимонена сильнее ускоряется окисью меди, чем восстановленной медью. Что бы получить С10Н20, необходимо углеводород гидрогенизирсвать дважды. С окисью никеля присоединение водорода к пинену пс д давлением идет быстро ей при более низкой температуре, чем над окисью меди; в обеих случаях получается ментан. [35]
Процесс заключается в окислении охлажденного водного раствора амина со взвешенной в нем восстановленной медью кислородом, который заметно адсорбируется. [36]
 |
Прибор для определения азота обычным микрометодом ( по Дюма. [37] |
Эти три слоя являются постоянным наполнением и меняются только после того, как восстановленная медь потемнеет. [38]
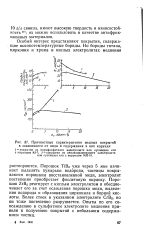 |
Прочностные характеристики медных покрытий. [39] |
Порошок TiB2 уже через 5 мин начинает выделять пузырьки водорода, частицы покрываются порошком восстановленной меди, электролит постепенно приобретает фиолетовую окраску. Порошок ZrB2 реагирует с кислым электролитом и обесцвечивает его за счет осаждения порошка меди, выделения водорода и образования цирконила и борной кислоты. Более стоек в указанном электролите СгВа, но он тоже постепенно разрушается. [40]
В образцах катализатора, выгруженных по окончании опытов, предварительно восстановленных, значительно больше восстановленной меди по сравнению с аналогичными образца-ми, применявшимися в окисной форме. [41]
Непосредственно за постоянным наполнением можно помещать также слой крупной окиси меди ( перед восстановленной медью), причем окись меди должна выступать на 3 - 5 см за пределы длинной горелки. [42]
Непосредственно за постоянным наполнением можно помещать также слой крупной окиси меди ( перед восстановленной медью), причем окись меди должна выступать на 3 - 5 см за пределы длинной горелки. [43]
Недавняя работа двух японских химиков, изучавших хлорирование нафталина при разных температурах в присутствии восстановленной меди, делает вероятным такое течение реакции, при котором медь ( в виде своего хлорного соединения) содействует в первую очередь образованию продуктов присоединения. [44]
Из других реагентов, применявшихся для проведения бекма-новской перегруппировки, можно отметить хлористый тионил, восстановленную медь, скелетный никелевый катализатор и фтористый водород. Хлористый тионил обычно применяется в эфире, хлороформе или бензоле и вызывает перегруппировку кетоксимов на холоду, так же как и пятихлористый фосфор. [45]
Страницы: 1 2 3 4