Мезопорфирин
Cтраница 1
Мезопорфирин C34H3804N4 получается в результате мягкого восстановления гемина или протопорфирина йодистым водородом или каталитически. [1]
При окислении мезопорфирина хромовой кислотой получаются метилэтилмалеинимид и так называемая гематиновая кислота. [2]
Гидрирование двух активных двойных связей протопорфирина приводит к мезопорфирину. [3]
При обработке гемина иодистоводородной кислотой в уксусной кислоте образуется мезопорфирин IX; винильные группы гемина восстанавливаются в этильные. Если же вместо иодистоводородной кислоты взять бромйстоводородную, получается гематопорфирин, содержащий две оксиэтильные лруппы вместо винильных. При декарбоксилировании мезопорфириеа получается этиопорфирин. [4]
В литературе опубликована только одна константа устойчивости металлопорфирина [69], а именно для реакции взаимодействия Zn ( II) с диметиловым эфиром мезопорфирина ( Р2 -) с образованием ZnP. Величина lg / С приблизительно равна 29 - цифра, которая достигается только макроциклическими лигандами ( разд. Малочисленность данных для равновесий этих реакций несомненно связана с исключительной медленностью их протекания, поскольку иногда необходимы месяцы для достижения равновесия при комнатной температуре. [5]
При обработке порфирина бромистоводородной кислотой удаляются две молекулы цистеина и возникает гематопорфирин; следовательно, два остатка цистеина были присоединены тиоэфирными связями к а-уг-леродным атомам этильных групп мезопорфирина. Порфирин с легко получается при реакции цистеина с протопорфирином IX путем присоединения сульфгидрильных групп к винильным. [6]
При реокислении эти водородные атомы не возвращаются к своим первоначальным положениям; так как в то же время 2 водородных атома остаются у винильной группы, то конечным результатом восстановления и реокисления явится изомеризация, причем первоначальный хлорин или форбин превращаются в изомерный мезопорфирин. [7]
Протопорфирин имеет три вида р-заместителей - винил, метил и пропионовый остаток - вследствие чего число возможных изомеров увеличивается до пятнадцати. Протопорфирин может перейти в мезопорфирин при превращении винильных групп в этильные. Фишеру) оказался изомером того же типа, что и метиловый эфир естественного протопорфирина, в связи с чем последний получил обозначение также под номером IX. С целью упрощенного изображения структурных формул различных порфиринов Лемберг и Легге ( 1949) предложили символ, в котором четыре угла соответствуют четырем азотам пиррольных колец, другие четыре - четырем метиновым мостикам между пиррольными кольцами. Восемь заместителей в р-положении пиррольных колец связаны пунктирными линиями с углеродными атомами центрального кольца, от которого они отделены р-карбоновыми атомами пиррольных колец. [8]
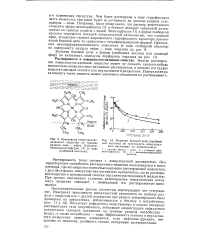 |
Влияние боковой цепи ( карбоно-вой кислоты на зависимость поверхностного натяжения от концентрации. [9] |
Чем более растворима в воде гидрофильная часть молекулы, тем выше будет ее активность на границе раздела углеводород - вода. Например, было обнаружено, что раствор диметилового сложного эфира мезопорфирина IX в бензоле обладает умеренной активностью на границе раздела с водой. Мезопорфирин IX в форме свободной кислоты отличается большей поверхностной активностью, чем сложный эфир, вследствие сильнее выраженного гидрофильного характера пропио-новой боковой цепи по сравнению с этерифицированной формой. [10]
Цитохром d ( полосы поглощения 630, 552 и 518 нм) выполняет роль конечной оксидазы у Aerobacter aerogenes и аэробных культур некоторых других бактерий. Каталитическое гидрирование с последующим окислением дает порфирин, похожий по свойствам на мезопорфирин. При восстановлении иодистоводородной кислотой получается порфирин, подобный 2-оксиэтил - 4-этилдейтеропорфирину. Наличие гидроксильной группы показано также бумажной хроматографией: Rf при хроматографии в системе керосин - пропанол ниже, чем у аналогичного хлорина, не имеющего гидроксильной группы ( мезохлорин), и возрастает при ацетилиро-вании. Присоединение диазоуксусного эфира показывает наличие винильной группы. [11]
Таким образом, не всегда образование комплекса железа с порфирином приводит к повышению активности. Это выражается также и в том, что порфирин, как и эфир дейтеропор-фирина или мезопорфирин, сильно тормозит реакцию. [12]
Формулы ( 32), ( 33) отличаются от широко применяемых, предложенных в Руководстве [65] коэффициентами пересчета: 0 476 для ванадиловых, 0 315 для никелевых порфиринов. Эти коэффициенты были выведены в 1955 г. на основе сравнения концентрации и интенсивности поглощения растворов в ближнем ультрафиолете синтетического свободного мезопорфирина с последующим пересчетом в видимую область для длинноволновой а-полосы. [13]
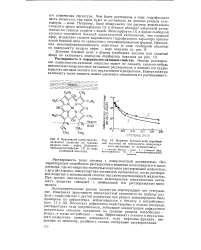 |
Влияние боковой цепи ( карбоно-вой кислоты на зависимость поверхностного натяжения от концентрации. [14] |
Чем более растворима в воде гидрофильная часть молекулы, тем выше будет ее активность на границе раздела углеводород - вода. Например, было обнаружено, что раствор диметилового сложного эфира мезопорфирина IX в бензоле обладает умеренной активностью на границе раздела с водой. Мезопорфирин IX в форме свободной кислоты отличается большей поверхностной активностью, чем сложный эфир, вследствие сильнее выраженного гидрофильного характера пропио-новой боковой цепи по сравнению с этерифицированной формой. [15]
Страницы: 1 2